
 的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是( )A.若某温度下,反应后 =11,则溶液中 =11,则溶液中 = = |
| B.参加反应的氯气的物质的量等于0.5amol |
C.改变温度,反应中转移电子的物质的量ne的范围: amol≤ne≤ amol≤ne≤ amol amol |
D.改变温度,产物中KC1O3的最大理论产量为 amol amol |
 =11,假设c(Cl-)=11,则c(ClO-)=1,根据氧化还原反应中电子转移数目相等可知1×11=1×1+5c(ClO3-),c(ClO3-)=2,则溶液中
=11,假设c(Cl-)=11,则c(ClO-)=1,根据氧化还原反应中电子转移数目相等可知1×11=1×1+5c(ClO3-),c(ClO3-)=2,则溶液中 =
= ,正确;B.在反应后产物中K与Cl原子个数比为1:1,因为n(KOH)=amol,所以参加反应的氯气的物质的量等于0.5amol,正确;C.改变温度,若反应后产物完全是KCl、KClO,发生反应:Cl2+2KOH="KCl+" KClO+H2O则转移电子的物质的量是
,正确;B.在反应后产物中K与Cl原子个数比为1:1,因为n(KOH)=amol,所以参加反应的氯气的物质的量等于0.5amol,正确;C.改变温度,若反应后产物完全是KCl、KClO,发生反应:Cl2+2KOH="KCl+" KClO+H2O则转移电子的物质的量是 amol,若反应后产物完全是KCl、KClO3,发生反应:3Cl2+6KOH="5KCl+" KClO3+3H2O,则转移电子的物质的量是
amol,若反应后产物完全是KCl、KClO3,发生反应:3Cl2+6KOH="5KCl+" KClO3+3H2O,则转移电子的物质的量是 amol。因此反应中转移电子的物质的量ne的范围:
amol。因此反应中转移电子的物质的量ne的范围: amol≤ne≤
amol≤ne≤ amol,正确。D.改变温度,若完全转化为产物KC1O3,则达到最大值,的最大理论产量为
amol,正确。D.改变温度,若完全转化为产物KC1O3,则达到最大值,的最大理论产量为 amol,错误。
amol,错误。

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源:不详 题型:单选题
| A.BaCl2溶液和K2SO4溶液反应 |
| B.点燃H2和O2的混合气体 |
| C.NaOH溶液和CuSO4溶液反应 |
| D.Fe放入盐酸中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用SO2漂白纸浆和草帽辫 |
| B.用氯化铁溶液腐蚀印刷线路板上的铜膜 |
| C.用牺牲阳极的阴极保护法防止金属被腐蚀 |
| D.高温下用焦炭还原SiO2制取粗硅 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.上述灼烧过程的尾气回收后可用来制硫酸 |
| B.上述过程中,由6 mol CuFeS2制取6 mol Cu时共消耗15 mol O2 |
| C.在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化产物与还原产物的物质的量比1:6 |
| D.在反应2Cu2O+Cu2S===6Cu+SO2↑中,只有Cu2O作氧化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
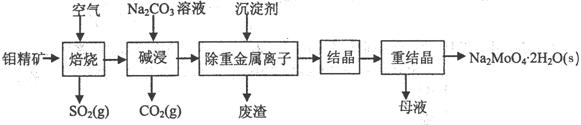 (1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
(1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
 Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。
Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
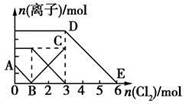
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中n(FeBr2)=3 mol |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+):n(I-):n(Br-)=3:1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
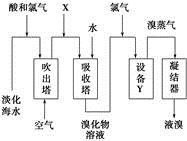
| A.X为SO2气体,也可将SO2换成Na2SO3 |
| B.设备Y为蒸馏塔 |
| C.在提取溴的过程中一定有Br-被氧化 |
| D.工业上每获得1 mol Br2,需要消耗Cl2的体积最多为44.8 L(标准状况下) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com