
【题目】下列物质既是钠盐,又是硫酸正盐的是( )
A.NaHSO4
B.Na2SO4
C.Na2SO3
D.Na2S2O3
科目:高中化学 来源: 题型:
【题目】茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示。下列说法正确的是
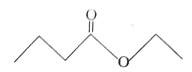
A. X难溶于乙醇
B. 酒中的少量丁酸能抑制X的水解
C. X的分子式为C6H10O2
D. 分子式为C4H8O2且官能团与X相同的物质共有5种(不考虑立体异构)
【答案】B
【解析】X是醇,易溶于酒精,故A错误;X水解产物是丁酸,所以丁酸能抑制X的水解,故B正确;X的分子式为C6H12O2,故C错误;分子式为C4H8O2且官能团与X相同的物质有HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3COOCH2CH3、CH3CH2COOCH3共4种,故D错误。
【题型】单选题
【结束】
5
【题目】W、X、Y、Z为原子序数依次增大的短周期主族元素,W、X处于不同周期,原子的最外层电子数X比Y多一个但比Z少一个,原子的电子层数X比Y、Z少一层。下列说法正确的是
A. 原子半径的大小为:Z>Y>X>W
B. 若Y、Z的核电荷数之和为X的4倍,则X、Z的气态氢化物的沸点:前者低于后者
C. 元素的非金属性:Y>Z
D. 若X的单质为常见的非金属导体,则Y的简单离子能破坏水的电离平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)(1)已知在448℃时,反应H2(g)+I2(g)2HI(g)ΔH<0的平衡常数K1为49,则该温度下反应2HI(g)H2(g)+I2(g)的平衡常数K2为______;反应1/2H2(g)+1/2I2(g)HI(g)的平衡常数K3为_______.
(2)在某一密闭容器中发生上述反应,改变反应的某一条件(混合气体的总物质的量不变),造成容器内压强增大,则下列说法中正确的是_____
A.容器内气体的颜色变深,混合气体的密度增大
B.平衡不发生移动
C.I2(g)的转化率增大,H2的平衡浓度变小
D.改变条件前后,速率图象如图所示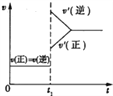
(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=______.
(2)该反应为______反应(填“吸热”或“放热”).
(3)能判断该反应达到化学平衡状态的依据是______.
A.容器中压强不变 B.混合气体中c(CO)不变
C.V(H2)正=V(H2O)逆 D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(H2)=c(CO)c(H2O),判断此时温度为______℃.
(5)在800℃时,发生上述反应,某时刻测得容器内各物质的浓度分别为c(CO2)=2mol/L (H2)=1.5mol/L 、 c(CO)=1mol/L 、 c(H2O)=3mol/L,则下一时刻,反应向_________填“正反应”或“逆反应”)方向进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包白色固体粉末,可能含有CuSO4、Na2SO4、(NH4)2CO3、BaCl2、NH4Cl 、KCl中的一种或几种。现做如下实验:
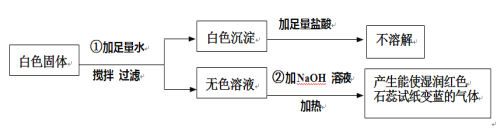
根据上述实验现象判断:
(1)原白色固体中一定不含________,一定含有________,可能含有________。
(2)写出①中生成白色沉淀的化学反应方程式__________________________。
(3)写出②中化学反应方程式__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格。
(演示实验)将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中。
(学生回答)该反应的化学方程式___________________________。
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
(假设猜想)针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想是____。
(实验探究)(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有___________。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,全班同学一致确定猜想二是正确的.
(评价反思)老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①实验操作中的错误是____________________。
②实验方案中也有一个是错误的,错误的原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R 是其中的五种元素。下列说法正确的是
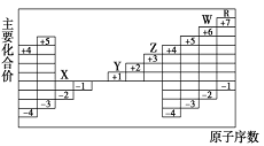
A. 离子半径: Y+>X2-
B. Y+、Z3+、W2-、R-在水中能大量共存
C. 氢化物的稳定性: H2W>H2X
D. 工业上利用电解熔融态YR和Z2X3的方法制取金属Y和乙单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
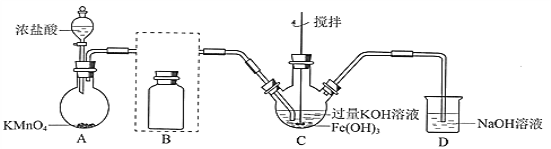
①A为氯气发生装置。A中反应方程式是___________________________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂 :______________________________
③C中得到紫色固体和溶液。C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH![]() 2K2FeO4+6KCl+8H2O,另外还有____________________________________(写离子方程式)。
2K2FeO4+6KCl+8H2O,另外还有____________________________________(写离子方程式)。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
i.由方案Ⅰ中溶液变红可知a中含有_______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由__________________________________________产生(用方程式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________________________。
②根据K2FeO4的制备实验得出:氧化性Cl2_______FeO42-(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com