
【题目】某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.由图中所给数据进行分析: 
(1)该反应的化学方程式为;
(2)反应从开始至2分钟末,用Z表示该反应的平均反应速率;
(3)反应达平衡时X的转化率: .
【答案】
(1)3X+Y?2Z
(2)0.05mol.L﹣1 . min﹣1
(3)30%
【解析】解:(1)由图象可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,当反应进行到2min时,△n(X)=0.3mol,△n(Y)=0.1mol,△n(Z)=0.2mol,则△n(X):△n(Y):△n(Z)=3:1:2,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为:3X+Y2Z,故答案为:3X+Y=2Z;(2)反应开始至2min末,Z的反应速率为:v= ![]() =
= ![]() =0.05mol/(Lmin),故答案为:0.05mol.L﹣1 . min﹣1;(3)反应达平衡时X的转化率=
=0.05mol/(Lmin),故答案为:0.05mol.L﹣1 . min﹣1;(3)反应达平衡时X的转化率= ![]() ×100%=30%,故答案为:30%. (1)根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式;(2)根据v=
×100%=30%,故答案为:30%. (1)根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式;(2)根据v= ![]() v进行计算;(3)转化率=
v进行计算;(3)转化率= ![]() ×100%.
×100%.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】下列离子的检验能达到预期目的是( )
A. 检验![]() :先滴加氯水,再滴加KSCN溶液,若变红,则有Fe2+
:先滴加氯水,再滴加KSCN溶液,若变红,则有Fe2+
B. 检验NH4+:先滴加NaOH溶液,加热,用湿润蓝色石蕊试纸检验,若变红,则有NH4+
C. 检验Cl—:先滴加AgNO3溶液,再滴加硝酸,若有白色沉淀,则有Cl—
D. 检验![]() :滴加硝酸,将生成的气体通入品红溶液,若品红溶液褪色,则有
:滴加硝酸,将生成的气体通入品红溶液,若品红溶液褪色,则有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两组热化学方程式中,有关△H的比较正确的是( ) ①CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H2
②NaOH(aq)+ ![]() H2SO4(浓)═
H2SO4(浓)═ ![]() Na2SO4(aq)+H2O(l)△H3
Na2SO4(aq)+H2O(l)△H3
NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l)△H4 .
A.△H1>△H2;△H3>△H4
B.△H1>△H2;△H3<△H4
C.△H1=△H2;△H3<△H4
D.△H1<△H2;△H3<△H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 某课外活动小组为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。

请回答下列问题:
(1)对于易燃、易爆、有毒的化学物质,往往会在其包装上面贴上危险警告标签。浓硫酸的危险警告标签是_______。
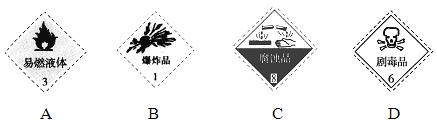
(2)装置A中发生反应的化学方程式为____________________________。
(3)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,则正确的操作顺序是_________________(用操作编号填写)
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(4)实验时,装置C中的现象为_______________________________________;
(5)当D中产生_______________________________________现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;
(6)Ⅰ若为检验浓硫酸与木炭在加热条件下生成的水蒸汽,可在装置__________之间加上一个盛有无水CuSO4的硬质玻璃管。
Ⅱ. Cu与浓硫酸反应可得硫酸铜溶液。某学习小组将铜屑放入一定浓度的硫酸中,加热并不断鼓入空气也可得硫酸铜溶液,其反应原理为2Cu+O2+2H2SO4![]() 2CuSO4+2H2O。现欲将12.8g铜完全溶解,加蒸馏水后得200 mL溶液。计算:
2CuSO4+2H2O。现欲将12.8g铜完全溶解,加蒸馏水后得200 mL溶液。计算:
(7)参加反应的氧气在标准状况下的体积是___________________ L。
(8)所得硫酸铜溶液的物质的量浓度是__________________ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A. 分散质粒子直径在1~100 nm之间B. 都是混合物
C. 都是无色、透明的溶液D. 都呈红褐色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列叙述正确的是( )
A.1L 0.5molL﹣1氨水中所含NH4+数为0.5NA
B.1mol Fe与足量氯气反应转移的电子数为2 NA
C.标准状况下,33.6LCO2约含有1.5NA个分子
D.1 mol ![]() 中含碳碳双键数为3 NA
中含碳碳双键数为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是C8H10(g)C8H8(g)+H2(g)△H>0 Ⅰ.某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内物质的量,得到数据如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2[来源:] | n3 |
n(C8H8)/mol | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
(1)当反应进行到20min时,该段时间内H2的平均反应速率是 .
(2)该温度下,该反应的化学平衡常数是 .
化学键 | C﹣H | C﹣C | C=C | H﹣H |
键能/kJmol1 | 412.5 | 348 | 612 | 436 |
(3)已知: 计算上述反应的△H=kJmol﹣1 . 若保持其他条件不变,用0.40mol H2(g)和0.40mol C8H8(g)合成C8H10(g),当有30kJ热量放出时,该反应中H2的转化率是 . 此时,该反应是否达到了平衡状态?(填“是”或“否”).
Ⅱ.工业上以高温水蒸气作为反应体系的稀释剂(不参与反应),C8H10(g)的平衡转化率与水蒸气的用量、体系的温度、压强的关系如图Ⅰ、图Ⅱ所示.
(4)由图Ⅰ可知,T1T2(填“大于”、“小于”或“等于”).
(5)由图Ⅱ可知,当其他条件不变时,水蒸气的用量越大,C8H10的平衡转化率将(填“越大”、“越小”或“不变”),原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氢氧化铁胶体中逐滴滴入下列某种溶液,出现的现象是先沉淀,后沉淀溶解.这种溶液是( )
A. 稀硫酸 B. 饱和硫酸镁溶液 C. 氯化钠溶液 D. 饱和硫酸铵溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com