
【题目】已知可逆反应X(g)+2Y(g)Z(g)△H<0,一定温度下,在体积为2L的密闭容器中加入4mol Y和一定量的X后,X的浓度随时间的变化情况如图所示,则下列表述正确的是( )

A. 达到平衡时,X、Y、Z物质的量之比为1:2:1
B. a点正反应速率大于逆反应速率
C. 反应达平衡时,降低温度可以实现c到d的转化
D. 该条件下,反应达平衡时,X平衡转化率为25%
【答案】B
【解析】
A、分析图象和题给信息可知,起始加入X的物质的量为1mol/L×2L=2mol,起始加入2molX、4molY,达到平衡时X的浓度为0.25mol/L,物质的量为0.25mol/L×2L=0.5mol,消耗X物质的量2﹣0.5mol=1.5mol,结合化学方程式计算得到消耗Y物质的量为3mol,生成Z物质的量为1.5mol,则达到平衡时,X、Y、Z物质的量之比=0.5:(4mol﹣3mol):1.5mol=1:2:3,故A错误;
B、由图象可知,a点尚未达到平衡状态,此时正反应速率大于逆反应速率,故B正确;
C、该反应的△H<0,为放热反应,降低温度,平衡正向移动,X的浓度减小,不能实现c到d的转化,故C错误;
D、利用三段式计算:X(g)+2Y(g)Z(g)
起始浓度(mol/L) 1 2 0
转化浓度(mol/L) 0.75 1.5 0.75
平衡浓度(mol/L) 0.25 0.5 0.75
X平衡转化率为75%,故D错误。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法肯定错误的是( )
A.某原子K层上只有一个电子
B.某原子M层上的电子数为L层上电子数的4倍
C.某离子M层上和L层上的电子数均为K层的4倍
D.某离子的核电荷数与最外层电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磺酰氯(SO2Cl2)是一种重要的有机合成试剂,主要用作氯化剂或氯磺化剂,也用于制造医药品、染料、表面活性剂等。实验室可利用SO2与Cl2反应制取少量SO2Cl2,所需装置如图所示(部分装置略):

已知:①Na2SO3+H2SO4![]() Na2SO4+H2O+SO2↑。
Na2SO4+H2O+SO2↑。
②SO2Cl2的熔点为-54.1℃,沸点为69.1℃,密度为1.67g/mL。它在常温下较稳定、遇水剧烈水解,100℃以上易分解。
回答下列问题:
(1)检查装置A气密性的操作是___________。
(2)选择实验装置(A~E)并连接接口(a~h)顺序:(A-a)___________(b-B-c)___________(h-E)(装置可重复使用)。
(3)B装置中的冷凝管需连接冷凝水,它应从___________(填“m”或“n”)接入。
(4)实验完成后装置D中可能观察到的现象是___________,产生该现象的原因是___________。
(5)设计如下实验,以检验SO2Cl2产品中是否溶有杂质。
①组装仪器,检查气密性;
②添加试剂抽取8.0mL液体产品,组装仪器;
③___________,缓慢推动注射器活塞将液体产品全部推入锥形瓶中,观察到的实验现象有___________;
④充分反应后,过滤、洗涤、干燥、称量固体质量为23.3g,表明液体产品中溶有___________,其理由是___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解NaB(OH)4溶液制备H3BO3的原理如图所示,下列叙述错误的是( )

A. M室发生的电极反应式:2H2O﹣4e﹣=O2↑+4H+
B. a、c为阴离子交换膜,b为阳离子交换膜
C. N室中:a%<b%
D. 每生成1mol H3BO3,则有1mol Na+进入N室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对![]() 溶液进行下列操作,观察到的现象与
溶液进行下列操作,观察到的现象与![]() 水解有关的是
水解有关的是![]()
![]()
A. 滴加NaOH溶液有沉淀产生 B. 加热蒸干灼烧得到红棕色固体
C. 通入![]() 气体有沉淀产生 D. 滴加KSCN试液溶液变红
气体有沉淀产生 D. 滴加KSCN试液溶液变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3。请结合图示回答下列问题:

(1)图1中一定为饱和溶液的是_____。
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为甲___乙。(大于、等于、小于)
(3)图3中表示乙的溶解度曲线是____(填曲线代码);P点表示的含义是_____。
(4)由图3知,30℃时,将20g甲固体溶于20g水,所得溶液的溶质质量分数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从酯类化合物A出发,一定条件下可发生如下的物质相互转化。完成下列填空:
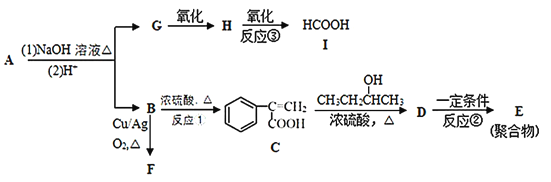
![]() 化合物G的名称是______,C中含氧官能团的名称是______。
化合物G的名称是______,C中含氧官能团的名称是______。
![]() 反应
反应![]() 的反应类型是______,反应
的反应类型是______,反应![]() 所需试剂与条件是______。
所需试剂与条件是______。
![]() 书写反应
书写反应![]() 的化学方程式______
的化学方程式______
![]() 写出A的结构简式______。
写出A的结构简式______。
![]() 写出一种C的苯环上只有一个侧链并可发生水解的同分异构体的结构简式______。
写出一种C的苯环上只有一个侧链并可发生水解的同分异构体的结构简式______。
![]() 设计一条由
设计一条由![]() 为原料制备
为原料制备![]() 的合成路线__________________。
的合成路线__________________。![]() 合成路线常用的表示方式为:
合成路线常用的表示方式为:![]() 目标产物
目标产物![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据科技日报网报道南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现丙烯醇高效、绿色合成。丙烯醇及其化合物可合成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的丙烯醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的电子排布式为____________________________________________。
(2)1 mol CH2=CH-CH2OH中σ键和π键的个数比为___________,丙烯醇分子中碳原子的杂化类型为___________。
(3)丙醛(CH3CH2CHO的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是______________________。
(4)羰基镍[Ni(CO)4]用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是___________。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]-和[Ni(CN)4]2-等。[Ni(NH3)6]2+中心原子的配位数是___________ ,与SCN-互为等电子体的分子为___________。
(6)“NiO”晶胞如图所示。

①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为___________。
②已知:氧化镍晶胞密度为dg/cm3,NA代表阿伏加德罗常数的值,则Ni2+半径为___________nm(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现需配制0.1mol/LNaOH溶液450mL,这是某同学转移溶液的示意图。

(1)仪器c使用前必须____。
(2)①图中的错误是____。除了图中给出的的仪器和托盘天平外,为完成实验还需要的仪器有:____。
②根据计算得知,需称出NaOH的质量为____g
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)____。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,反复颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的___,溶液注入容量瓶前需恢复到室温,这是因为____;
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?若没有进行A操作____;若加蒸馏水时不慎超过了刻度线___;若定容时俯视刻度线___;若配制完成后发现砝码和药品颠倒了(未使用游码),则结果____;若用天平称固体时,砝码上沾有油污,则所配制的溶液浓度将_____。
(5)若实验过程中加蒸馏水时不慎超过了刻度线应如何处理?____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com