
某原电池的总反应的离子方程式是Zn + Cu2+ = Zn2+ + Cu,该原电池的组成正确的是:
| A | B | C | D | |
| 正极 | Zn | Ag | Cu | Cu |
| 负极 | Cu | Cu | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | CuSO4 | FeCl2 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列叙述能肯定金属A 比金属B更活泼的是
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子的电子层数比B原子多
C.1 mol A从酸中置换出H2比1 mol B多
D.常温下,A能从酸中置换出氢气,而B不能
查看答案和解析>>
科目:高中化学 来源: 题型:

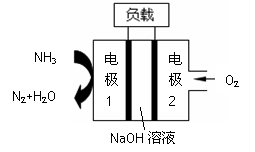
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电
池示意图如右,有关说法正确的是
A.电池工作时,Na+ 向负极移动
B.电子由电极2经外电路流向电极1
C.电池总反应为:4NH3+3O2=2N2+6H2O
D.电极2发生的电极反应为:O2+ 4H + + 4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
按右图装置通入X气体,并在管P处点燃,实验结果是澄清石灰水变浑浊,则X、Y可能是 ( )。
A.H2和Fe2O3
B.CO和CuO
C.H2 和Na2CO3
和Na2CO3
D.CO和Na2CO3

查看答案和解析>>
科目:高中化学 来源: 题型:
下列微粒半径大小比较正确的是:
A.Na+<Mg2+<Al3+<O2- B.S2->Cl->Na+>Al3+
C.Na<Mg<Al<S D.Ca<Rb<K<Na
查看答案和解析>>
科目:高中化学 来源: 题型:
哈伯因发明了由氮气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2 2NH3 。下列有关说法正确的是:
2NH3 。下列有关说法正确的是:
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
C.达到化学平衡时,反应则停止进行
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列叙述中正确的是( )
A.14 g乙烯和丙烯的混合物中总原子数为3NA
B.常温下11.2 L甲烷气体含有甲烷分子数为0.5NA
C.5.6 g铁与足量的稀硫酸反应失去电子数为0.3 NA
D.0.1 mol·L-1的氢氧化钠溶液中含钠离子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各种溶液中,能大量共存的无色透明的离子组
A.PH=0的溶液:CH3COO- 、NO3-、SO42-、I-
B.C(H+)=10-14mol/L的溶液中:Na+ 、AlO2-、S2-、SO32-
C.酸性环境下:Na+、Cu2+、NO3-、SO42-、
D.pH=7的溶液中:K+ 、Na+ 、Fe3+ 、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题
(1)甲同学运用沉淀法测定样品中NaOH的含量。甲同学选用的药品除样品外,还应有
▲ ,实验中应测定的数据有 ▲ 。
(2)乙同学运用滴定法测定样品中NaOH的含量。
①用分析天平准确称取该样品5.360g,全部溶于水配制成1000.0mL的溶液。用碱式滴定管取其中20.00mL放在锥形瓶中,滴加几滴甲基橙做指示剂。用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 ▲ 。滴定终点的现象是 ▲ 。
②下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 ▲ (填写序号)
 A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
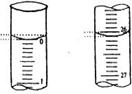
③若滴定开始和结束时,酸式滴定管中的液面如右图所示:
开始 结束
则起始读数为 ▲ mL,终点读数 ▲ mL;
(3)某学生根据三次实验分别记录有关数据如下:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 第一次 | 20.00 | 0.00 | 26.01 | |
| 第二次 | 20.00 | 1.56 | 30.30 | |
| 第三次 | 20.00 | 0.22 | 26.21 |
请选用其中合理的数据列式计算出该样品中NaOH的质量百分含量。(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com