
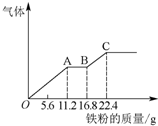
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示.下列分析或结果错误的是( )| A、H2SO4的物质的量浓度应为5mol/L |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、原混合酸中NO3-的物质的量为0.4 mol |
| 22.4g |
| 56g/mol |
| 0.4mol |
| 0.1L |
| 11.2g |
| 56g/mol |


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案科目:高中化学 来源: 题型:
| A、单位时间内生成n mol O2,同时生成2n mol NO2 |
| B、混合气体的密度不再改变 |
| C、混合气体的颜色不再改变 |
| D、O2的浓度不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,则该溶液一定含有SO42- |
| B、向某溶液中加入CCl4,CCl4层显紫色,证明原溶液中存在I2 |
| C、向某溶液中加入稀盐酸,产生的气体能使澄清石灰水变浑浊,则溶液中一定含有CO32- |
| D、向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,说明H2SiO3的酸性强于H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H2SO4 |
| NaOH |
| NaOH |
| H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com