
【题目】在环境保护越来越重视的今天,大型工厂搬离主城区是一个趋势。某一大型钢铁厂在生产时经常产生大量红棕色的烟,你估计这一空气污染物最有可能是( )
A.氧化镁粉尘
B.氧化铁粉尘
C.二氧化硅粉尘
D.氧化铝粉尘
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)某原子含有 6 个质子和 8 个中子,用核素符号表示该原子__________;(用元素符号表示)
(2)写电子式:HClO:____;NH4+:_____;写结构式:CCl4:_____;CS2:_____;
(3)画出钙原子的原子结构示意图:____;画出溴离子的离子结构示意图:____;
(4)用电子式表示氯化钠的形成过程:_________________________
(5)按要求排序:
下列离子半径由大到小的顺序是:S2- ;Al3+ ;Na+ ;F- ;______________
下列物质熔沸点由高到低的顺序是:H2O;Na2O;H2Se;I2 ;______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到目的的是
目的 | 操作 | |
A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
B. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
C. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A. NaCl和HCl B. CO2和SiO2 C. SO2和H2O D. CCl4和NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100 mol·L-1的NaOH溶液滴定10.00 mL浓度均为0.100 mol·L-1 的盐酸和 CH3COOH溶液。利用传感器测得滴定过程中溶液 的电导率如图所示。下列说法不正确的是
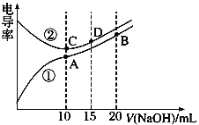
A. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)= 0.0500 mol·L-1
B. 曲线②代表滴定CH3COOH溶液的曲线
C. 在相同温度下,A、B、C三点溶液中水的电离程度: A>C>B
D. B点溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008奥运吉祥物福娃,其外材为纯羊毛线,内充物为无毒的聚酯纤维(如图)。下列说法正确的是

A. 羊毛与聚酯纤维的化学成分相同
B. 该聚酯纤维的单体为对苯二甲酸和乙醇
C. 聚酯纤维和羊毛一定条件下均能水解
D. 聚酯纤维属于纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明同学设计了如图所示装置来探究铜跟浓硫酸的反应。
先关闭活塞a,加热至烧瓶中不再有气泡产生时,反应停止,此时烧瓶中铜片仍有剩余。再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢消失。

(1)请写出上述过程A装置中所涉及的化学反应方程式。
________________________
_________________________
(2)实验中加热至烧瓶中不再有气泡产生时,反应停止,此时烧瓶中铜片为什么有剩余?请简述其原因是:___________。
(3)老师认为实验中B装置设计有误,请你帮助小明进行修改:___________。
(4)B中所收集到的气体既具有氧化性又具有还原性,请写出该气体与O2反应的化学方程式:______。
(5)装置C中应盛放____溶液,其作用是:____,所发生的离子方程式为:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“价——类”二维图是学习元素化合物知识的好方法,依据图中氮元素及其化合物的转化关系,回答问题:
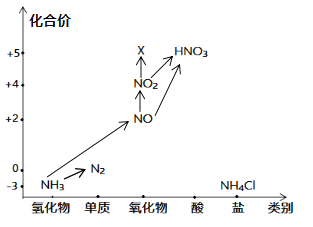
(1)图中,X的化学式为_____,从N元素的化合价看,X具有_____性(“氧化”、“还原”)。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为______。
②下列试剂不能用于干燥NH3的是______(填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
③请写出NH3→NO的化学方程式_____________ 。
④工业生产中利用氨水吸收SO2和NO2,原理如下图所示:
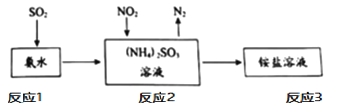
请写出反应2中NO2被吸收过程的化学反应程式是_____。
(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。SCR(选择性催化还原)工作原理:

①已知尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出SCR催化反应器中NH3还原NO2的化学方程式:_________。
②尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60g·mol 1)含量的方法如下:取ag尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1mLc1mol·L1 H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容的容器中进行反应:2HI![]() H2+I2(正反应为吸热反应),反应物的浓度由0.1 mol/L降到0.06 mol/L需要20 s,那么由0.06 mol/L降到0.036 mol/L所需时间为
H2+I2(正反应为吸热反应),反应物的浓度由0.1 mol/L降到0.06 mol/L需要20 s,那么由0.06 mol/L降到0.036 mol/L所需时间为
A. 等于10 s B. 等于12 s C. 大于12 s D. 小于12 s
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com