
 A��B��C��D��Ԫ�����ڱ���ǰ36��Ԫ�أ����ǵĺ˵�����������ڶ�����Ԫ��Aԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2������3���ܼ���Bԭ�ӵ������p����ĵ���Ϊ������ṹ��C�ǵؿ��к�������Ԫ�أ�D�ǵ�������Ԫ�أ���ԭ�Ӻ�����������������ԭ����ͬ�����������Ӿ���������ش��������⣺
A��B��C��D��Ԫ�����ڱ���ǰ36��Ԫ�أ����ǵĺ˵�����������ڶ�����Ԫ��Aԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2������3���ܼ���Bԭ�ӵ������p����ĵ���Ϊ������ṹ��C�ǵؿ��к�������Ԫ�أ�D�ǵ�������Ԫ�أ���ԭ�Ӻ�����������������ԭ����ͬ�����������Ӿ���������ش��������⣺���� A��B��C��D����ǰ36��Ԫ�أ����ǵĺ˵�����������ڶ�����Ԫ��Aԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2������3���ܼ�����ԭ�Ӻ�������Ų�Ϊ1s22s22p2����AΪ̼Ԫ�أ�C�ǵؿ��к�����ߵ�Ԫ�أ�����C��OԪ�أ�Bԭ�ӵ������p����ĵ���Ϊ�����ṹ�����������Ų�Ϊ2s22p3����BΪNԪ�أ�D�ǵ�������Ԫ�أ���ԭ�Ӻ�����������������ԭ����ͬ�����������Ӿ���������DԪ��ԭ�Ӹ���������ֱ�Ϊ2��8��18��1����29��CuԪ�أ��ݴ˽��
��� �⣺A��B��C��D����ǰ36��Ԫ�أ����ǵĺ˵�����������ڶ�����Ԫ��Aԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2������3���ܼ�����ԭ�Ӻ�������Ų�Ϊ1s22s22p2����AΪ̼Ԫ�أ�C�ǵؿ��к�����ߵ�Ԫ�أ�����C��OԪ�أ�Bԭ�ӵ������p����ĵ���Ϊ�����ṹ�����������Ų�Ϊ2s22p3����BΪNԪ�أ�D�ǵ�������Ԫ�أ���ԭ�Ӻ�����������������ԭ����ͬ�����������Ӿ���������DԪ��ԭ�Ӹ���������ֱ�Ϊ2��8��18��1����29��CuԪ�أ�
��1��C��N��OԪ����ͬһ����Ԫ�أ�ͬһ����Ԫ��������ҵ�һ�����ܳ��������ƣ���NԪ��ԭ��2p�ܼ��ǰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ��ʵ�һ������C��O��N��Nԭ�Ӻ�������Ų�ʽ1s22s22p3����3��������ͬ�ĵ��ӣ�DΪCuԪ�أ�ԭ�Ӻ��������Ϊ29����ԭ�Ӻ�������Ų�ʽΪ��1s22s22p63s23p63d104s1��
�ʴ�Ϊ��3��1s22s22p63s23p63d104s1��
��2��H2CO3��Cԭ������������ȫ���ɼ���û�йµ��Ӷԣ���1��C=O˫����2��C-O�������ӻ������ĿΪ3����ȡsp2�ӻ���NO3-��Nԭ���γ�3���Ҽ����µ��Ӷ�=$\frac{5+1-2��3}{2}$=0����ӦΪƽ�������Σ�
�ʴ�Ϊ��sp2��ƽ�������Σ�
��3����CN-��Cԭ�Ӽ�1������ɻ���1��Nԭ�ӣ��ɵõĵȵ�����N2��CN-���γ�C��N������1��CN-����2���м�����1mol CN-�к��еĦм�����Ϊ2NA��
�ʴ�Ϊ��2NA��
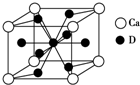
��4���ɾ����ṹ��֪��Caԭ�Ӵ��ڶ��㣬�����к���Caԭ����ĿΪ8��$\frac{1}{8}$=1��Cuԭ�Ӵ��ھ����ڲ������ϡ����ģ�������Cu��ĿΪ1+4��$\frac{1}{2}$+4��$\frac{1}{2}$=5���ʸúϽ���Ca��Cu��ԭ�Ӹ�����Ϊ1��5��
�ʴ�Ϊ��1��5��
��5����H2O�����ͷų�����ʱ������һ�������Ӿ��н�ǿ�������ԣ�����������SO2ˮ��Һ��Ӧ���ӷ���ʽΪ��2H2O++SO2=4H++SO42-��
�ʴ�Ϊ��2H2O++SO2=4H++SO42-��
���� ������Ԫ�ص��ƶ�Ϊ���壬�����˵����ܡ��ӻ����ۡ����ӽṹ����������Ų����ɡ����������֪ʶ�㣬�Ƕ����ʽṹ֪ʶ���ۺϿ��飬���ض�֪ʶǨ�Ƶ����á��������������������飬ע��ͬһ����Ԫ�صĵ�һ����������ԭ�����������������������ƣ�����A�塢VA�����ͬ��������Ԫ�صģ�


 ���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢� | C�� | �ڢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ������=ԭ�Ӻ��������� | |
| B�� | Ԫ�ص�����=ԭ������ | |
| C�� | Ԫ�����ڱ�����������=ԭ�ӵ����������� | |
| D�� | Ԫ�����ڱ���������=ԭ�ӵĵ��Ӳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ռ����ʳƷ����� | B�� | �����Ӵ�Ǧ��о�����Ǧ�ж� | ||
| C�� | �������������ζƷ | D�� | ��˿����Ҫ�ɷ��ǵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
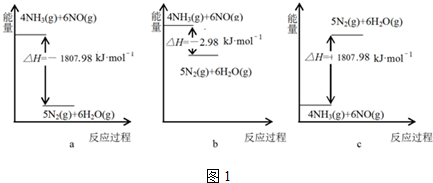
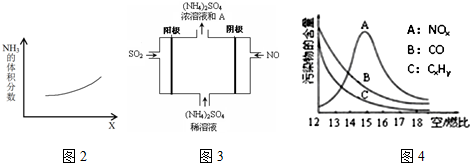
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
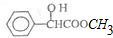
| A�� | ����ʽΪC9H10O3 | |
| B�� | ���Է���ȡ����Ӧ���ӳɷ�Ӧ��������Ӧ�ͻ�ԭ��Ӧ | |
| C�� | 1mol������������4mol H2�����ӳɷ�Ӧ | |
| D�� | �䱽���ϵĶ��ȴ��ﹲ�����ֽṹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | OH-+2CO32-+3H+��2HCO3-+H2O | B�� | 2OH-+CO32-+3H+��HCO3-+2H2O | ||
| C�� | 2OH-+CO32-+4H+��CO2��+3H2O | D�� | OH-+CO32-+3H+��CO2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
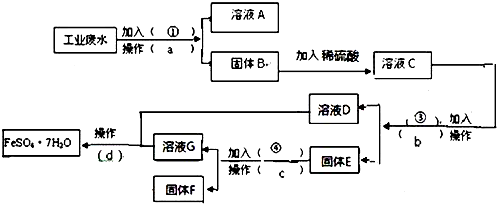
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
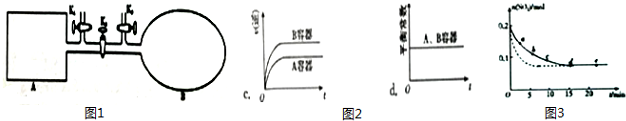
| ��� | a | b | c | d | e |
| n��SO2��/mol | 0.16 | 0.12 | 0.09 | 0.07 | 0.07 |
| t/min | 2 | 5 | 8 | 15 | 22 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com