
ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ�������ָʾ��������д���пհף�
(1)�ñ�������ζ������NaOH��Һʱ����������ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע��________��ֱ�������һ���������Һ�ɻ�ɫ��Ϊ��ɫ����______Ϊֹ��
(2)���в����п���ʹ����NaOH��Һ��Ũ����ֵƫ�͵���________(����ĸ���)��
A����ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B���ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
(3)���ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼ��ʾ������ʼ����Ϊ________mL���յ����Ϊ________mL��
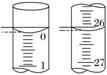
����������Һ�����Ϊ________mL��
(4)ijѧ������3��ʵ��ֱ��¼�й��������±���
| �ζ����� | ����NaOH��Һ�����/mL | 0.100 0 mol·L��1��������/mL | ||
| �ζ�ǰ�̶� | �ζ���̶� | ��Һ���/mL | ||
| ��һ�� | 25.00 | 0.00 | 26.11 | 26.11 |
| �ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
| ������ | 25.00 | 0.22 | 26.31 | 26.09 |
�����ϱ�������ʽ�����NaOH��Һ�����ʵ���Ũ�ȡ�
�𰸡�(1)��ƿ����Һ��ɫ�仯���ڰ�����ڲ���ɫ
(2)D��(3)0.00��26.10��26.10
(4)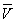 ��
��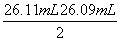 ��26.10 mL��c(NaOH)��
��26.10 mL��c(NaOH)��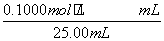 ��0.104 4 mol·L��1
��0.104 4 mol·L��1
����������c(NaOH)�ͽ���������ʱӦ���ݹ�ʽ��c(NaOH)��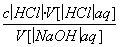 ������c(NaOH)��������V[(HCl)aq]�ٴ��빫ʽ������������ʱ��Ҫ����ʵ�ʲ�����ÿһ������V[(HCl)aq]��V[(NaOH)aq]��Ӱ�죬����Ӱ��c(NaOH)��
������c(NaOH)��������V[(HCl)aq]�ٴ��빫ʽ������������ʱ��Ҫ����ʵ�ʲ�����ÿһ������V[(HCl)aq]��V[(NaOH)aq]��Ӱ�죬����Ӱ��c(NaOH)��
(1)��������к͵ζ�ʵ��Ĺ淶������
(2)�������ڲ���ȷ������������������ζ���δ�ñ�������ϴ���ڱڸ���һ��ˮ���ɽ����������ϡ�ͣ�������ͬ���ļ������������ƫ���ƫ�ߣ��ü�ʽ�ζ���ȡ���Ĵ���NaOH��Һ�����ʵ���һ��ȷ����������ƿ��ˮ�ļ��벻Ӱ��OH�������ʵ�����Ҳ�Ͳ�Ӱ���������ų����ݣ�Һ����½����ʶ�ȡV��ƫ���ƫ�ߣ���ȷ����(���߲���)�ʹ������(ʵ�߲���)��ͼ��ʾ��

(3)����ʱ����Һ�����͵�Ϊ����
(4)��������ñ������ƽ��ֵ
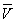 ��
��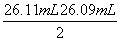 ��26.10 mL(�ڶ���ƫ��̫����ȥ)��
��26.10 mL(�ڶ���ƫ��̫����ȥ)��
c(NaOH)��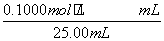 ��0.104 4 mol·L��1��
��0.104 4 mol·L��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪1 g������ȫȼ������Һ̬ˮʱ�ų�����143 kJ��18 gˮ�������Һ̬ˮ�ų�44 kJ����������������������±���
| O===O(g) | H—H | H—O | |
| 1 mol��ѧ������ʱ��Ҫ���յ�����/kJ | 496 | x | 463 |
�����xΪ(����)
A��920 B��557
C��436 D��188
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����(����)
A��S(g)��O2(g)===SO2(g)����H1��S(s)��O2===SO2(g)����H2����H1����H2
B��C(ʯī��s)===C(���ʯ��s)����H����1.9 kJ·mol��1������ʯī��ȡ���ʯ�ķ�Ӧ�����ȷ�Ӧ�����ʯ��ʯī�ȶ�
C��NaOH(aq)��HCl(aq)===NaCl(aq)��H2O(l)����H����57.4 kJ·mol��1����20 g NaOH��ϡ��Һ��ϡ������ȫ��Ӧ���ų�������Ϊ28.7 kJ
D��2C(s)��O2(g)===2CO(g)����H����221 kJ·mol��1����̼��ȼ���ȵ���110.5 kJ·mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��pH��ֽ����Һ��pHʱӦע��ʲô���⣿��¼����ʱ��Ҫע��ʲô���Ƿ����pH��ֽ�ⶨ��ˮ��pH?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶��£���һ�����0.1 mol·L��1�Ĵ�����Һ����μ����Ũ�ȵ�NaOH��Һ����Һ��pOH(pOH����lg[OH��])��pH�ı仯��ϵ��ͼ��ʾ����(����)

A��M����ʾ��Һ�ĵ�������ǿ��Q��
B��N����ʾ��Һ��c(CH3COO��)>c(Na��)
C��M���N����ʾ��Һ��ˮ�ĵ���̶���ͬ
D��Q������NaOH��Һ��������ڴ�����Һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£������йص������Һ��������ȷ����(����)
A��ͬŨ�ȡ�ͬ�����ǿ����ǿ����Һ��Ϻ���Һ��pH��7
B����10 mL pH��a��������100 mL pH��b��Ba(OH)2��Һ��Ϻ�ǡ���кͣ���a��b��13
C����pH��10��Ba(OH)2��Һ��pH��13��NaOH��Һ�������ϣ���Ϻ���Һ��pH��10.7(��֪lg 2��0.3)
D��pH��2��������pH��12�İ�ˮ�������Ϻ�������Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ǰ������Ԫ��ԭ�Ӻ�������Ų��ص㣬�ش��������⣺
(1)��Χ���Ӳ���2��δ�ɶԵ��ӵ���________����3��δ�ɶԵ��ӵ���________��
(2)δ�ɶԵ���������������ȵ�Ԫ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Զ��������ԭ����ӽ�������һ��������ϵ������(����)
A���ȱ����С B���ȱ�С����
C����С D��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com