
【题目】如图,A、B、C、D、E是长式元素周期表中的5种元素(不包括镧系和锕系)。下列说法不正确的是

A. D、E 原子序数之差可能是8、18或32 B. B、C原子序数之差一定是2
C. A、E 原子序数之差可能为2 D. B、D原子序数之差不可能是7
【答案】AC
【解析】若A位于ⅢB元素之左,则A不可能是第2周期的Li、Be元素;因为A若为Li,则不存在B;A若为Be,则不存在C;A不是第2周期元素,则E不是第3周期元素,由序数之差的左上右下规律及只有2、3两周期含8种元素知,D、E原子序数之差不可能为8, D、E上原子序数之差可以是18或32;A错误;B、C之间仅隔有一种E元素,故其原子序数之差一定为2;B正确;由题给五元素的位置关系可以看出,A不是第1周期元素,因为A若为氢元素则其为最左一族,那么就不应有B。A若为氦元素,则其为最右一族,那么就不应有C。既然A不是氢元素,则A、E原子序数之差不可能为2; C错误;由于D、E原子序数之差可能是18或32 ,B、E相差1,且在E的左侧,因此,B、D原子序数之差为19或33,不可能相差7,D正确;正确选项AC。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:
【题目】高锰酸钾可用于生活消毒,是中学化学常见的氧化剂.工业上,用软锰矿制高锰酸钾的流程如下: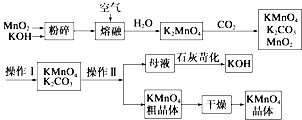
请回答下列问题:
(1)该生产中需要纯净的CO2气体.写出实验室制取CO2的化学方程式 .
(2)KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是(填字母).a.75%酒精 b.双氧水 c.苯酚 d. 84消毒液(NaClO溶液)
(3)写出二氧化锰和氢氧化钾熔融物中通入空气时发生的主要化学反应的方程式: .
(4)上述流程中可以循环使用的物质有、(写化学式).
(5)测定高锰酸钾样品纯度采用硫酸锰滴定:向高锰酸钾溶液中滴加硫酸锰溶液,产生黑色沉淀.当溶液由紫红色刚好褪色且半分钟不恢复,表明达到滴定终点.写出该反应的离子方程式: .
(6)已知:常温下,Ksp[Mn(OH)2]=2.4×10﹣13 . 工业上,调节pH可以沉淀废水中Mn2+ , 当pH=10时,溶液中c(Mn2+)= .
(7)操作Ⅰ的名称是;操作Ⅱ根据KMnO4和K2CO3两物质在溶解性上的差异,采用(填操作步骤)、趁热过滤得到KMnO4粗晶体.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于晶体的下列说法正确的是( )
A.只要含有金属阳离子的晶体就一定是离子晶体
B.离子晶体中一定含金属阳离子
C.在共价化合物分子中各原子都形成8电子结构
D.分子晶体的熔点不一定比金属晶体熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值.下列说法正确的是( )
A.1 molCu和足量热浓硫酸反应可生成NA个SO3分子
B.3mol单质Fe完全转变为Fe3O4 , 失去8 NA个电子
C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA
D.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4mol SO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2+O22SO3测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时各物质的浓度;
(2)平衡时SO2的转化率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列颜色变化与氧化还原反应有关的是( )
A.氨气遇到HCl气体后产生白烟
B.品红溶液通入SO2气体后褪色
C.湿润的淀粉碘化钾试纸遇Cl2变蓝
D.在无色火焰上灼烧NaCl火焰呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.在Na2CO3、NaHCO3两溶液中,离子种类不相同
B.在等体积、等物质的量浓度的Na2CO3、NaHCO3两溶液中,阳离子总数相等
C.在NaHCO3和Na2CO3混合溶液中一定有c(Na+)+c(H+)=c(HCO ![]() )+c(OH﹣)+2c(CO
)+c(OH﹣)+2c(CO ![]() )
)
D.在NaHCO3和Na2CO3混合溶液中一定有2c(Na+)=3[c(HCO ![]() )+c(CO
)+c(CO ![]() )+c(H2CO3)]
)+c(H2CO3)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、L、M、R、Q是短周期主族元素,部分信息如下表所示:
X | Y | Z | M | R | Q | |
原子半径 | 0.186 | 0.074 | 0.099 | 0.143 | ||
主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
其他 | 阳离子无核外电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(1)X和M的原子可构成18电子的分子,该分子的结构式为_______ .
(2)Z与Q相比,金属性较强的是_______ (用元素符号表示),下列事实能证明一结论的是_______ (填字母序号)。
a.Q的熔点比Z的熔点高,Q的硬度比Z的硬度大
b.Z与冷水反应迅速,而Q与冷水几乎不反应
c.Z的最高价氧化物对应水化物是强碱,而Q的最高价氧化物对应水化物具有两性
(3)与Y元素同主族的短周期元素E在自然界中存在多种核素,它们之间的关系互为_______,其中用于测定一些文物年代的核素的符号为_______ 。
(4)写出Z2M2的电子式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( ) 
A.温度:T1>T2>T3
B.平衡常数:K(a)>K(c) K(b)=K(d)
C.正反应速率:v(a)>v(c) v(b)>v(d)
D.平均摩尔质量:M(a)<M(c) M(b)>M(d)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com