
【题目】常温下,某酸H3A水溶液中含A的各种粒子的分布分数(平衡时某种粒子的浓度占各粒子浓度之和的分数)与pH的关系图如下所示,下列说法正确的是
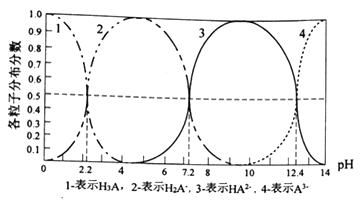
A. NaH2A水溶液呈碱性
B. H3A溶液中存在:c(H+)=c(OH-)+c(H2A-)+1/2c(HA2-)+1/3c(A3-)
C. 向H3A溶液中加入一定量的NaOH溶液至pH=5时,c(HA2-)/c(H3A)=100.6
D. 向H3A溶液中加入氨水使pH从5→9发生的主要离子反应是:H2A-+OH-![]() HA2-+H2O
HA2-+H2O
【答案】C
【解析】
从图像可知H3A为弱酸,存在电离平衡,H3A![]() H2A-+H+,Ka1=[c(H2A-)c(H+)]/c(H3A)=10-2.2,H2A-
H2A-+H+,Ka1=[c(H2A-)c(H+)]/c(H3A)=10-2.2,H2A-![]() HA2-+H+ Ka2=[ c(HA2-) c(H+)]/ c(H2A-)=10-7.2,H2A-+H2O
HA2-+H+ Ka2=[ c(HA2-) c(H+)]/ c(H2A-)=10-7.2,H2A-+H2O![]() H3A+OH-水解常数为K= c(H3A) c(OH-)/ c(H2A-),据此分析;
H3A+OH-水解常数为K= c(H3A) c(OH-)/ c(H2A-),据此分析;
水的离子积常数为KW= c(H+) c(OH-)=10-14,所以K= c(H3A) KW/ c(H2A-) c(H+)=KW/ Ka1=10-11.8;Ka2/K=[ c(HA2-)c(H+)]/ c(H2A-)=10-7.2/10-11.8=104.6>1,所以电离大于水解,所以NaH2A水溶液呈酸性,故A项错误;B.HA2-![]() A3-+H+;H2O
A3-+H+;H2O![]() H++OH-,根据质子守恒c(H+)=c(OH-)+c(H2A-)+2c(HA2-)+3c(A3-),故B错误;C.因为Ka1=[c(H2A-)c(H+)]/c(H3A)=10-2.2,Ka2=[ c(HA2-) c(H+)]/ c(H2A-)=10-7.2, Ka1. Ka2=[c(HA2-)C2(H+)]/ c(H3A),(Ka1. Ka2)/ C2(H+)=c(HA2-)/ c(H3A),当溶液至pH=5时,c(H+)=10-5,c(HA2-)/ c(H3A)= (10-2.2 10-7.2)/ 10-10=10-0.6,故C正确;D.因为氨水为弱电解质,所以在离子反应方程式中不能拆,故D错误。综上,本题选C。
H++OH-,根据质子守恒c(H+)=c(OH-)+c(H2A-)+2c(HA2-)+3c(A3-),故B错误;C.因为Ka1=[c(H2A-)c(H+)]/c(H3A)=10-2.2,Ka2=[ c(HA2-) c(H+)]/ c(H2A-)=10-7.2, Ka1. Ka2=[c(HA2-)C2(H+)]/ c(H3A),(Ka1. Ka2)/ C2(H+)=c(HA2-)/ c(H3A),当溶液至pH=5时,c(H+)=10-5,c(HA2-)/ c(H3A)= (10-2.2 10-7.2)/ 10-10=10-0.6,故C正确;D.因为氨水为弱电解质,所以在离子反应方程式中不能拆,故D错误。综上,本题选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】离子键、共价键、金属键、范德华力是微粒之间的不同作用力,下列物质中含有上述任意两种作用力的是( )
①Na2O2 ②SiO2 ③氦气 ④金刚石 ⑤NH4Cl ⑥白磷
A.①②④B.①③⑥C.①⑤⑥D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。
请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 ΔH=+88.6 kJ·mol-1
ΔH=+88.6 kJ·mol-1
则M、N相比,较稳定的是 。
(2)已知CH3OH(l)的燃烧热为238.6 kJ·mol-1,CH3OH(l)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a 238.6(填“>”、“<”或“=”)。
O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a 238.6(填“>”、“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式: 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是________(填序号)。
A. Cl2 B. 淡水 C. 烧碱 D. 食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是______。
(3)下图是从海水中提取镁的简单流程。

工业上常用于沉淀Mg2+的试剂A的俗名是________,氢氧化镁转化为MgCl2的离子方程式是_______。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是________________。步骤②加热煮沸一会的目的是_______________________________
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_____________________。反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈________色。从碘的提取CCl4提取碘可以用_______的方法。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种高分子化合物(Ⅵ)是目前市场上流行的墙面涂料之一,其合成路线如下(反应均在一定条件下进行):
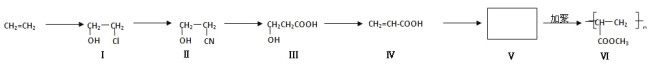
回答下列问题:
(1)化合物Ⅲ中所含官能团的名称是___________________、_______________________。
(2)化合物Ⅲ生成化合物Ⅳ的同时,副产物为____________________________。
(3)CH2=CH2与溴水反应方程式:_______________________________。
(4)写出合成路线中从化合物Ⅳ到化合物Ⅴ的反应方程式:_____________________。
(5)下列关于化合物Ⅲ、Ⅳ和Ⅴ的说法中,正确的是_____________。
A化合物Ⅲ可以发生氧化反应
B化合物Ⅲ不可以与NaOH 溶液反应
C化合物Ⅳ能与氢气发生加成反应
D化合物Ⅲ、Ⅳ均可与金属钠反应生成氢气
E化合物Ⅳ和Ⅴ均可以使溴的四氯化碳溶液褪色
(6)写出化合物Ⅰ与氧气在Cu催化下反应的产物______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对尼古丁和苯并[a]芘的分子组成与结构描述正确的是 ( )

A. 尼古丁为芳香族化合物
B. 尼古丁的分子式为C10H14N2
C. 苯并[a]芘分子中含有苯环结构单元,是苯的同系物
D. 尼古丁分子中的所有碳原子一定不在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是现代文明的原动力,通过化学方法开辟新能源和提高能量转化率。
请回答下列问题:
(1)已知一定条件下白磷转化为红磷释放出能量,故白磷比红磷稳定性______(填“强”、“弱”)
(2)化学反应的本质是旧的化学键断裂,新的化学键形成。已知断开1molH﹣H键、1molN≡N键、lmolN﹣H键分别需要吸收的能量为436kJ、946kJ、391kJ。那么生成1mo1 NH3需要________(填“放出”或“吸收”)__________kJ 的热量。
(3)化学电源在生产生活中有着广泛的应用。
①为了探究化学反应中的能量变化,某同学设计了如下两个实验(如下图)。
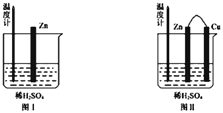
下列说法正确的是___________(填序号)
A.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
B.图Ⅱ中产生气体的速率比Ⅰ快
C.图Ⅰ中温度计的示数高于图Ⅱ的示数
D.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温
②燃料电池是一种高效、环境友好的供电装置。以氢气为燃料的电池中,电解质溶液为氢氧化钾溶液,负极的反应式为_______________________,当外电路转移1.2mol电子,消耗的氧气的体积为_____________ L(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl﹣、SO42﹣、CO32﹣、AlO2﹣ 中的若干种离子,离子浓度均为 0.1molL﹣1.某同学进行了如下实验:

下列说法正确的是( )
A. 无法确定原试液中是否含有 Al3+、 Cl﹣
B. 滤液 X 中大量存在的阳离子有 NH4+、 Fe2+和 Ba2+
C. 无法确定沉淀 C 的成分
D. 原溶液中存在的离子为 NH4+、 Fe2+、 Cl﹣、 SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六苯乙烷为白色固体,其结构如下图。下列有关说法中不正确的是 ( )

A. 它是一种芳香烃,易溶于乙醚中
B. 它的分子式为C38H30,是非极性分子
C. 它的一氯代物只有一种
D. 在同一平面上的碳原子最多有14个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com