
 £®
£®·ÖĪö £Ø1£©ÖŹ×ÓŹżĻąĶ¬£¬ÖŠ×ÓŹż²»Ķ¬µÄŌ×Ó»„ĪŖĶ¬Ī»ĖŲ£»Ķ¬ÖÖŌŖĖŲŠĪ³ÉµÄ²»Ķ¬µ„ÖŹ£¬»„ĪŖĶ¬ĖŲŅģŠĪĢ壻
£Ø2£©Ņ»°ćĄ“Ėµ£¬»īĘĆ½šŹōŌŖĖŲÓė·Ē½šŹōŌŖĖŲŠĪ³ÉĄė×Ó¼ü£¬·Ē½šŹōŌŖĖŲÖ®¼äŠĪ³É¹²¼Ū¼ü£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ£Ø1£©A£®ŗģĮ×ŗĶ°×Į× ¾łŹĒPŌŖĖŲŠĪ³ÉµÄ²»Ķ¬ÖÖµ„ÖŹ£¬»„ĪŖĶ¬ĖŲŅģŠĪĢ壻
B£®ėŗĶė°¾łŹĒHŌŖĖŲµÄ²»Ķ¬ÖÖŌ×Ó£¬»„ĪŖĶ¬Ī»ĖŲ£»
C£®ĀČĘųŗĶŅŗĀČ¾łŹĒĀČĘųµ„ÖŹ£¬ŹōÓŚĶ¬ÖÖĪļÖŹ£»
D£®±łŗĶøɱł£¬Ņ»øöŹĒĖ®£¬Ņ»øöŹĒ¶žŃõ»ÆĢ¼£¬Į½ÕߏōÓŚ²»Ķ¬µÄĪļÖŹ£»
E£®ŃõĘųŗĶ³ōŃõ ¾łŹĒOŌŖĖŲŠĪ³ÉµÄ²»Ķ¬ÖÖµ„ÖŹ£¬»„ĪŖĶ¬ĖŲŅģŠĪĢ壻
F£®13CŗĶ14C£¬ÖŹ×ÓŹżĻąĶ¬£¬ÖŠ×ÓŹż²»Ķ¬£¬»„ĪŖĶ¬Ī»ĖŲ£¬
¹Ź“š°øĪŖ£ŗBF£»AE£»
£Ø2£©¢ŁĀČ»Æļ§ŗ¬Ąė×Ó¼üŗĶN-H¼«ŠŌ¼ü£¬ĪŖĄė×Ó»ÆŗĻĪļ£»
¢Śŗ¤ĘųĪŖµ„Ō×Ó·Ö×Ó£¬²»ŗ¬ÓŠ»Æѧ¼ü£»
¢ŪĀČ»ÆĆ¾ÖŠÖ»ŗ¬ÓŠĄė×Ó¼ü£»
¢Ü¶žŃõ»ÆĢ¼ÖŠÖ»ŗ¬ÓŠ¹²¼Ū¼ü£»
¢ŻĀČ»ÆÄĘÖ»ŗ¬ÓŠĄė×Ó¼ü£»
¢Ž¹żŃõ»ÆÄĘÖŠÄĘĄė×ÓÓė¹żŃõøłĄė×ÓŠĪ³ÉĄė×Ó¼ü£¬ŃõŌ×ÓÖ®¼ä“ęŌŚ¹²¼Ū¼ü£»
ĘäÖŠ£ŗa£®Ö»ŗ¬Ąė×Ó¼üµÄĪļÖŹŹĒ¢Ū¢Ż£»¹Ź“š°øĪŖ£ŗ¢Ū¢Ż£»
b£®Ö»ŗ¬¹²¼Ū¼üµÄĪļÖŹŹĒ¢Ü£¬CO2ŹĒ¹²¼Ū»ÆŗĻĪļ£¬Ęä½į¹¹Ź½ĪŖO=C=O£¬Ģ¼Ō×ÓŗĶŃõŌ×ÓÖ®¼äÓŠ2¶Ōµē×Ó£¬Ęäµē×ÓŹ½ĪŖ £»
£»
¹Ź“š°øĪŖ£ŗ¢Ü£» £»
£»
c£®¼ČÓŠĄė×Ó¼üÓÖ¹²¼Ū¼üµÄŹĒ¢Ł¢Ž£»
¹Ź“š°øĪŖ£ŗ¢Ł¢Ž£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ¼ü£¬°ŃĪÕ»Æѧ¼üµÄŠĪ³É¼°ÅŠ¶ĻµÄŅ»°ć¹ęĀɵČĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā³£¼ūĪļÖŹÖŠµÄ»Æѧ¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “ĪĀČĖįµÄ½į¹¹Ź½H-Cl-O | |
| B£® | ĀČ»ÆÄʵķÖ×ÓŹ½£ŗNaCl | |
| C£® | F-µÄ×īĶā²ćµē×ÓÅŲ¼Ź½£ŗ2s22p5 | |
| D£® | D216OÖŠ£¬ÖŹĮæŹżÖ®ŗĶŹĒÖŹ×ÓŹżÖ®ŗĶµÄĮ½±¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4LH2OÖŠĖłŗ¬Ō×Ó×ÜŹżĪŖNA | |
| B£® | ÖŹĮæ¾łĪŖ7.8 gµÄNa2S”¢Na2O2¹ĢĢåÖŠŗ¬ÓŠµÄŅõĄė×ÓŹż¾łĪŖ0.1NA | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24 L Cl2ĶØČė×ćĮæH2O£¬×ŖŅʵĵē×ÓŹż¾łĪŖ0.1NA | |
| D£® | ³£ĪĀĻĀ£¬ÅضČĪŖ0.01mol/LµÄNa2CO3ČÜŅŗÖŠCO32-µÄŹżÄæĪŖ0.01 NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
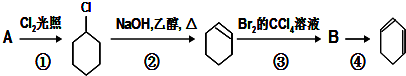
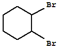 £»
£» +Cl2 $\stackrel{¹āÕÕ}{”ś}$
+Cl2 $\stackrel{¹āÕÕ}{”ś}$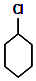 +HCl£®
+HCl£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH3COOH | B£® | Br2 | C£® | SO2 | D£® | NH4HCO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 ŅŃÖŖA”¢B”¢C”¢D”¢E”¢F¶¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒµÄŗĖµēŗÉŹżŅĄ“ĪµŻŌö£®BŌ×ÓµÄP¹ģµĄ°ė³äĀś£¬ŠĪ³ÉĒā»ÆĪļµÄ·ŠµćŹĒĶ¬Ö÷×åŌŖĖŲµÄĒā»ÆĪļÖŠ×īµĶµÄ£®DŌ×ӵƵ½Ņ»øöµē×Óŗó3P¹ģµĄČ«³äĀś£®A+±ČDŌ×ÓŠĪ³ÉµÄĄė×ÓÉŁŅ»øöµē×Ó²ć£®CÓėAŠĪ³ÉA2CŠĶĄė×Ó»ÆŗĻĪļ£®EµÄŌ×ÓŠņŹżĪŖ31£¬FÓėBŹōĶ¬Ņ»Ö÷×壬EÓėFŠĪ³ÉµÄ»ÆŗĻĪļ³£ÓĆÓŚÖĘŌģ°ėµ¼Ģ壮øł¾ŻŅŌÉĻŠÅĻ¢£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
ŅŃÖŖA”¢B”¢C”¢D”¢E”¢F¶¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒµÄŗĖµēŗÉŹżŅĄ“ĪµŻŌö£®BŌ×ÓµÄP¹ģµĄ°ė³äĀś£¬ŠĪ³ÉĒā»ÆĪļµÄ·ŠµćŹĒĶ¬Ö÷×åŌŖĖŲµÄĒā»ÆĪļÖŠ×īµĶµÄ£®DŌ×ӵƵ½Ņ»øöµē×Óŗó3P¹ģµĄČ«³äĀś£®A+±ČDŌ×ÓŠĪ³ÉµÄĄė×ÓÉŁŅ»øöµē×Ó²ć£®CÓėAŠĪ³ÉA2CŠĶĄė×Ó»ÆŗĻĪļ£®EµÄŌ×ÓŠņŹżĪŖ31£¬FÓėBŹōĶ¬Ņ»Ö÷×壬EÓėFŠĪ³ÉµÄ»ÆŗĻĪļ³£ÓĆÓŚÖĘŌģ°ėµ¼Ģ壮øł¾ŻŅŌÉĻŠÅĻ¢£¬»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČŻĘ÷ÄŚA”¢B”¢CµÄÅضČÖ®±ČĪŖ1£ŗ2£ŗ2 | |
| B£® | µ„Ī»Ź±¼äĻūŗÄ0.2 mol/L BĶ¬Ź±Éś³É0.2 mol/L C | |
| C£® | ČŻĘ÷ÄŚŃ¹Ēæ²»Ėꏱ¼ä±ä»Æ | |
| D£® | ČŻĘ÷ÄŚBµÄÅØ¶Č²»Ėꏱ¼ä±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com