
A、F的原子结构示意图: | ||
B、NH4Br的电子式: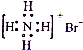 | ||
C、原子核内有l8个中子的氯原子:
| ||
| D、乙烯的结构简式:CH2CH2 |
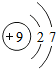 ,故A错误;
,故A错误;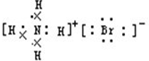 ,故B错误;
,故B错误;35 17 |


科目:高中化学 来源: 题型:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
| a | |||
| b | |||
| c | d | ||
| e |
| A、元素b位于ⅥA族,有+6、-2两种常见化合价 |
| B、五种元素中,元素e的性质最稳定 |
| C、原子半径有d>c>b |
| D、元素e参与形成的化合物可以作为一种半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | ||||
B、
| ||||
| C、含0.4molHCl的浓盐酸和足量的MnO2反应制Cl2,标准状况下得到2.24L Cl2 | ||||
| D、不能用淀粉碘化钾试纸鉴别氯气和溴蒸汽 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于45.3% |
| B、小于45.3% |
| C、等于45.3% |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuFeS2既是氧化剂又是还原剂,硫元素既被氧化又被还原 |
| B、每生成1mol SO2转移6mol电子 |
| C、SO2既是氧化产物又是还原产物,FeS只是还原产物 |
| D、每转移1.2 mol电子,有0.3 mol氧气被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 现有可逆反应:X(g)+Y(g)?2Z(g)+W(s)△H<0,RU 图a曲线表示X的转化率随时间的变化关系.若改变起始条件使反应按b曲线进行,可采取的措施是( )
现有可逆反应:X(g)+Y(g)?2Z(g)+W(s)△H<0,RU 图a曲线表示X的转化率随时间的变化关系.若改变起始条件使反应按b曲线进行,可采取的措施是( )| A、降低温度 |
| B、增大Y的浓度 |
| C、加入催化剂 |
| D、增大容器的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子式为C3H8与C6H14的两种有机物一定互为同系物 |
| B、具有相同通式的有机物不一定互为同系物 |
| C、分子式C4H10表示的物质必是纯净物 |
D、有机物 的名称:2,3,5-三甲基-4-乙基庚烷 的名称:2,3,5-三甲基-4-乙基庚烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
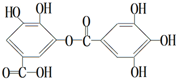
| A、该化合物的分子式为C14H10O10 |
| B、该分子中的所有碳原子一定在同一平面上 |
| C、遇FeCl3溶液显紫色因为该物质与苯酚属于同系物 |
| D、该物质在酸性条件下水解,产物只有1种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com