
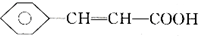 ),继而合成H的路线如下:
),继而合成H的路线如下: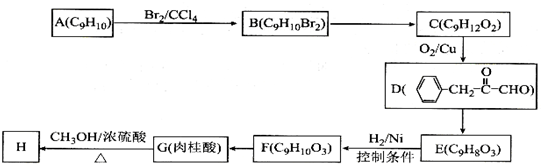
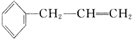 ,D中含有官能团的名称为羰基、醛基;
,D中含有官能团的名称为羰基、醛基; +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$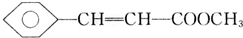 +H2O;
+H2O;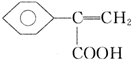 、
、 、
、 、
、 .
. 分析 C的不饱和度=$\frac{9×2+2-12}{2}$=4,C的不饱和度为4,结合D结构简式知,C中含有一个苯环,C结构简式为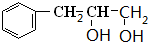 ,B发生取代反应或水解反应生成C,B结构简式为
,B发生取代反应或水解反应生成C,B结构简式为 ,A发生加成反应生成B,A结构简式为
,A发生加成反应生成B,A结构简式为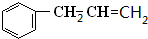 ;结合E分子式知,D发生氧化反应生成E,E结构简式为
;结合E分子式知,D发生氧化反应生成E,E结构简式为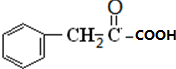 ,E发生加成反应结合F分子式知,F结构简式为
,E发生加成反应结合F分子式知,F结构简式为 ,F发生消去反应生成
,F发生消去反应生成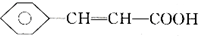 ,G发生酯化反应生成H,H结构简式为
,G发生酯化反应生成H,H结构简式为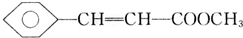 ,据此分析解答.
,据此分析解答.
解答 解:C的不饱和度=$\frac{9×2+2-12}{2}$=4,C的不饱和度为4,结合D结构简式知,C中含有一个苯环,C结构简式为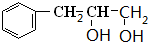 ,B发生取代反应或水解反应生成C,B结构简式为
,B发生取代反应或水解反应生成C,B结构简式为 ,A发生加成反应生成B,A结构简式为
,A发生加成反应生成B,A结构简式为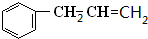 ;结合E分子式知,D发生氧化反应生成E,E结构简式为
;结合E分子式知,D发生氧化反应生成E,E结构简式为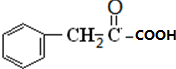 ,E发生加成反应结合F分子式知,F结构简式为
,E发生加成反应结合F分子式知,F结构简式为 ,F发生消去反应生成
,F发生消去反应生成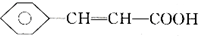 ,G发生酯化反应生成H,H结构简式为
,G发生酯化反应生成H,H结构简式为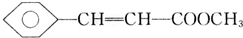 ,
,
(1)通过以上分析知,A的结构简式为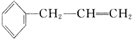 ,D中官能团是羰基、醛基,故答案为:
,D中官能团是羰基、醛基,故答案为: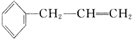 ;羰基、醛基;
;羰基、醛基;
(2)B需要在NaOH水溶液中发生取代反应生成C,F发生消去反应生成G,反应类型是消去反应,
故答案为:氢氧化钠的水溶液;消去反应;
(3)G发生酯化反应生成H,反应方程式为 +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$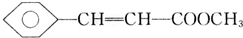 +H2O,
+H2O,
故答案为: +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$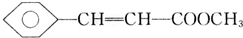 +H2O;
+H2O;
(4)F结构简式为 ,F中苯环能和氢气发生加成反应,所以1molF最多能和3mol氢气发生加成反应,故答案为:3;
,F中苯环能和氢气发生加成反应,所以1molF最多能和3mol氢气发生加成反应,故答案为:3;
(5)与肉桂酸互为同分异构体,且能使溴的四氯化碳溶液褪色说明含有碳碳不饱和键,还能与碳酸氢钠溶液反应,说明含有羧基,符合条件的同分异构体结构简式为 、
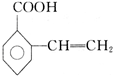
、 、
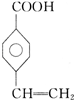
、 、
、 ,
,
故答案为: 、
、 、
、 、
、 .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识综合应用能力,根据某些物质的分子式、结构简式结合反应条件采用正逆结合的方法进行推断,正确推断各物质结构简式是解本题关键,难点是同分异构体结构简式确定,注意限制性条件,题目难度中等.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | Na2SO4 KNO3 Na2CO3 NH4Cl | B. | H2SO4 BaCl2 Na2SO4 NaOH | ||
| C. | MgCl2 AgNO3 KNO3 HCl | D. | NH4HCO3 NaOH NaCl HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇难溶于水 | B. | 乙烯可使酸性KMnO4溶液褪色 | ||
| C. | 乙酸的酸性比碳酸弱 | D. | 苯不能萃取碘水中的碘单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知0.1 mol•L-1的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,加少量烧碱溶液可使溶液中c(H+)/c(CH3COOH)值增大 | |
| B. | 25℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O?H++OH-逆向移动,c(H+)降低 | |
| C. | 取c(H+)=0.01mol/L的盐酸和醋酸各100mL,分别稀释2倍后,再分别加入 0.03g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 | |
| D. | 常温下,将pH=11的Ba(OH)2溶液加水稀释10倍后,溶液的pH=12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
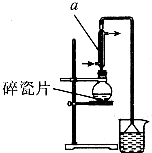 醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备1一溴丁烷的反应和实验装置如下:
醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备1一溴丁烷的反应和实验装置如下:| 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | |
| 正丁醇 | -89.53 | 117.25 | 0.81 |
| 1-溴丁烷 | -112.4 | 101.6 | 1.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH3+Cl2$\stackrel{光}{→}$CH3CH2Cl+HCl | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | 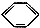 +Br2$\stackrel{Fe}{→}$ +Br2$\stackrel{Fe}{→}$ Br+HBr Br+HBr | |
| D. | CH2═CH2+Br2→CH2Br-CH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在上述条件下,SO2可能100%的转化为SO3 | |
| B. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| C. | 达到平衡时,SO2与SO3的浓度保持不变 | |
| D. | 为了提高SO2的转化率,可以适当提高O2的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
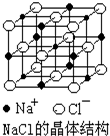 NaCl晶体结构如图所示,现测知NaCl晶体中Na+与Cl-平均距离为a cm,该晶体密度为ρg•cm-3,则阿伏加德罗常数可表示为( )
NaCl晶体结构如图所示,现测知NaCl晶体中Na+与Cl-平均距离为a cm,该晶体密度为ρg•cm-3,则阿伏加德罗常数可表示为( )| A. | $\frac{0.585}{4{a}^{3}ρ}$ | B. | $\frac{5.85}{8{a}^{3}ρ}$ | C. | $\frac{58.5}{2{a}^{3}ρ}$ | D. | $\frac{58.5}{{a}^{3}ρ}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com