
对于放热反应H2+Cl2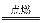 2HCl,下列说法中,正确的是( )。
2HCl,下列说法中,正确的是( )。
A.生成物所具有的总能量高于反应物所具有的总能量
B.反应物所具有的总能量高于生成物所具有的总能量
C.断开1molH-H键和1molCl-Cl键所吸收的总能量大于形成2molH-Cl键所放出的能量
D.该反应中,化学能只转变为热能
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源:2015-2016学年浙江省高一下期中化学试卷(解析版) 题型:选择题
向某恒容密闭容器中通入N2和H2,在500 ℃时,使反应:N2(g)+3H2(g) 2NH3(g) △H<0达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
2NH3(g) △H<0达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
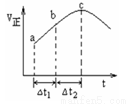
A.反应在c点达到平衡状态
B.△t1=△t2时,N2的转化量:a~b段小于b~c段
C.C点反应放出的热量达到最大
D.反应物浓度:a点小于b点
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀
B. 配制一定物质的量浓度的溶液,定容时俯视刻度线,会使所配溶液浓度偏高
C. 二氧化硅不与强酸反应,可用石英作为反应容器制取氢氟酸
D. 燃着的镁条伸入盛满二氧化碳的集气瓶中,不能继续燃烧
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分,针对表中标出的①~⑩元素,请回答有关问题:
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ⑨ | ④ | ⑤ | ⑩ | ⑥ | ⑦ | ⑧ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为_______________;
(2)表中金属性最强的元素是 (用元素符号表示,下同),非金属性最强的元素是 ,可作半导体材料的是 元素的单质;
(3)表中能形成两性氢氧化物的元素是__________,写出该元素的单质与⑨的最高价氧化物的水化物反应的化学方程式___________________________________________ ;
(4)⑨的最高价氧化物的水化物所含化学键类型 ;
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是__________ (填化学式);
(6)元素①的最高价氧化物的电子式_______,④元素与⑦元素形成化合物的电子式________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
某元素原子的质量数为A,它的阳离子Rn+核外有x个电子,w克这种元素的原子核内中子数为( )
A.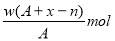 B.
B.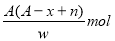
C.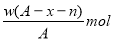 D.
D.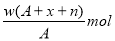
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
同周期的IIA族元素与IIIA族元素核电荷数相差不可能是( )
A.1 B.11 C.17 D. 25
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆生产建设兵团二中高一下期中化学试卷(解析版) 题型:填空题
IA、B、C、D四种元素的核电荷数均小于18,A元素原子核外只有1个电子;B是地壳中含量最多的元素;B、C可形成两种化合物CB和CB2,C的最高正价与最低负价绝对值相等,CB有毒,CB2可用于灭火;D+具有与Ne原子相同的电子层结构。
(1)试判断A、B、C、D四种元素的名称。A______,B_____,C______,D______。
(2)C在周期表中的位置是 。
(3)由B、D两种元素组成的D2B2型化合物的电子式为_______,CB2的电子式 为________。
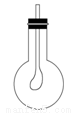
(4)如右图所示,在烧瓶中收集满CB2气体,用带导管(导管一端事先绑好一个气球)的胶塞紧,当打开胶塞迅速倒入浓的A、B、D三种元素组成的化合物的溶液后,立即塞紧胶塞振荡,可观察到_____,原因是_____________。
II(9分)下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
主族K] 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | [m] | ⑩ |
(1)在最高价氧化物的水化物中,酸性最强的化合物的分子式是: ,碱性最强的化合物的电子式是: 。
(2)最高价氧化物是两性氧化物的元素是 ;写出它的氧化物与氢氧化钠反应的离子方程式 。
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式 ,该化合物是由 (填“极性”“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是______(要求用离子符号表示)。
(6)元素③的氢化物常温下和元素⑦的单质反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆生产建设兵团二中高一下期中化学试卷(解析版) 题型:选择题
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是

A.最简单气态氢化物的热稳定性:R>Q
B.最高价氧化物对应水化物的酸性:Q<W
C.原子半径:T>Q>R
D.R的气态氢化物的水溶液显酸性
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:选择题
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数,B原子核内质子数和中子数相等。下列叙述不正确的是( )

A.B为第二周期的元素 B.C为VA元素
C.三种元素都为非金属元素 D.C元素最高正价为+7价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com