
【题目】对于可逆反应A (g)+2B(g)![]() 2C (g)(正反应为吸热反应)达到平衡时,要使正反应速率降低,且使A的浓度增大,应采取的措施是
2C (g)(正反应为吸热反应)达到平衡时,要使正反应速率降低,且使A的浓度增大,应采取的措施是
A. 增大压强 B. 减少B的浓度 C. 减少A的浓度 D. 升高温度
科目:高中化学 来源: 题型:
【题目】古语道:“人要实,火要虚”。此话的意思是做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺。从燃烧的条件看,“火要虚”的实质是( )
A. 增大可燃物的热值 B. 提高空气中氧气的含量
C. 提高可燃物的着火点 D. 增大可燃物与空气的接触面积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: 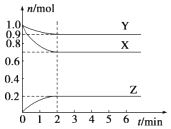
(1)该反应的化学方程式为 .
(2)反应开始至2min,气体Z的反应速率为 .
(3)若X、Y、Z均为气体,反应达到平衡时,压强是开始时的倍;此时放出了a kJ的热量,则按(1)的反应方程式写成热化学反应方程式时,该反应的反应热△H= .
(4)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.已知:
化学键 | H﹣H | H﹣Cl | Cl﹣Cl |
键能/KJmol﹣1 | 436 | 431 | 242 |
工业上通过氢气在氯气中充分燃烧制取HCl气体,写出该反应的热化学反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气: 2NO+2CO ![]() 2CO2+N2 .
2CO2+N2 .
(1)写出CO2的结构式 , N2的电子式 .
(2)一定条件下,在容积固定的容器中进行上述反应,CO浓度与时间关系如图所示: 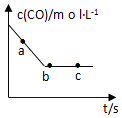
①则反应速率 ![]() (a)、
(a)、 ![]() (b)、
(b)、 ![]() (c)的大小关系是;
(c)的大小关系是;
②下列可说明反应到达图中c点的是;
A.NO、CO、CO2、N2的浓度比值保持2:2:2:1不变
B.CO的浓度不再改变
C.反应消耗2molNO的同时消耗1molN2
D.容器中的气体质量或物质的量保持不变
(3)为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究. 【资料查阅】
A.不同的催化剂对同一反应的催化效率不同;
B.使用等质量相同的催化剂时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
实验编号 | 实验目的 | T/℃ | NO初始浓度 | CO初始浓度 | 同种催化剂的比表面积 | 达平衡时所用的时间min |
Ⅰ | 参照实验 | 280 | 6.50×10﹣3 | 4.00×10﹣3 | 80 | t |
Ⅱ | 280 | 6.50×10﹣3 | 4.00×10﹣3 | 120 | 0.5t | |
Ⅲ | 360 | 6.50×10﹣3 | 4.00×10﹣3 | 80 | 0.2t |
【结论】①实验编号Ⅱ的实验目的为 .
②课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是 , 且反应速率将 . (填“增大”、“减小”、“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表的一部分,请回答心里问题: 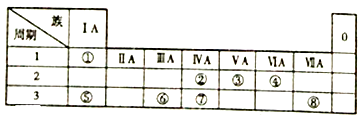
(1)若①和⑤可以形成原子个数比1:1的化合物,此时①显价.①和⑧形成的化合物的电子式为 .
(2)②和③的最高价含氧酸的酸性强弱顺序>(填分子式).
(3)④和⑦形成的常见化合物的晶体类型为 , 微粒间通过形成了该晶体.④和②形成的常见化合物的晶体类型为 , 微粒间通过形成了该晶体.
(4)⑥为材料的容器可以装运浓硫酸或浓硝酸的理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: 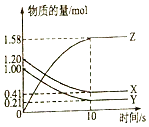
(1)反应的化学方程式为 .
(2)反应010s的化学反应速率v(Z)= .
(3)反应开始到10s,X的物质的量浓度减少了 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com