
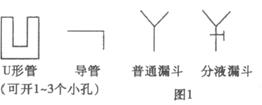
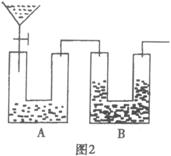
某同学用图2测定Na2CO3试样的纯度(杂质不与水反应),其中A容器中盛有Na2CO3样品10.0g,分液漏斗内盛有稀硫酸,B容器内为碱石灰固体。他利用碱石灰的增重求出纯净的Na2CO3质量,再求纯度。他重复正确操作了三次,结果数据出现了较大偏差(设原容器中CO2气体的含量可忽略不计,各容器内反应完全,下同)
(1)请你分析出现较大偏差的原因__________________________________________________。
通过仔细分析,该同学重新设计了一套实验装置(见图3)。(实验室中可供选择的试剂和药品还有Zn片、浓硫酸、NaOH溶液、CaCO3固体、蒸馏水)

(2)该同学新设计的装置仍不完整,应在_________处(填B或D)添加_________(写出装置及药品的名称)。
(3)A装置中分液漏斗所盛液体为_________,F装置在整套装置中的作用是_______________
_____________________________________________________________________。
(4)如果B、D内不设计任何装置而直接连通A、C、E,则实验结果将_________(填偏高、偏低、无影响)。
科目:高中化学 来源: 题型:
氯气是一种重要的化工原料。
(1)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 。
(2)资料显示:![]() 。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
①在该实验中,甲部分的装置是 (填字母);指出a中m仪器的名称 。
![]()
![]()
②乙装置中FeCl2溶液Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是(填加试剂的名称、至少填二种)方法 、
;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、清毒的物质。已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是 ;
(3)为测定漂白粉中Ca(ClO)2的质量分数,该小组将2.0g漂白粉配制成250mL溶液,取出25mL并向其中依次加入过量稀H2SO4、过量KI溶液,完全反应后,再滴入![]() 溶液:
溶液:![]() ,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。
,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:江西师大附中2010届高三第三次模拟考试理综化学 题型:实验题
氯气是一种重要的化工原料。
(1)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 。
(2)资料显示: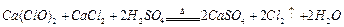 。某学习小组利用此原理设
。某学习小组利用此原理设 计如图所示装置制取氯气并探究其性质。
计如图所示装置制取氯气并探究其性质。
①在该实验中,甲部分的装置是 (填字母);指出a中m仪器的名称 。
|

 ②乙装置中FeCl2溶液Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是(填
②乙装置中FeCl2溶液Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是(填 加试剂的名称、至少填二种)方法 、
加试剂的名称、至少填二种)方法 、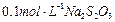 溶液:
溶液: ,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。
,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。查看答案和解析>>
科目:高中化学 来源:2013-2014学年甘肃省高三上学期期末考试理综化学试卷(解析版) 题型:填空题
最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。具体生产流程如图:
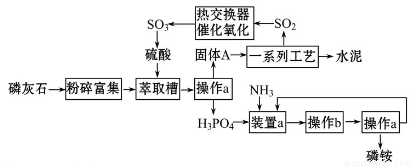
回答下列问题:
(1)操作a的名称是___________,实验室中进行此操作的非玻璃仪器或用品有________________;在实验室中操作b的名称是______________________。
(2)装置a中生成两种酸式盐,它们的化学式分别是_______________。
(3)依题意猜测固体A中一定含有的物质的化学式是____________________(结晶水部分不写)。
(4)热交换器是实现冷热交换的装置。化学实验中也经常利用热交换来实现某种实验目的,气、液热交换时通常使用的仪器是________________________。
(5)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2,微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是___________________。
A.NaOH溶液、酚酞试液????????????? B.KMnO4溶液、稀硫酸
C.碘水、淀粉溶液?????????????????? D.氨水、酚酞试液
查看答案和解析>>
科目:高中化学 来源:江西师大附中2010届高三第三次模拟考试理综化学 题型:实验题
氯气是一种重要的化工原料。
(1)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 。
(2)资料显示: 。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
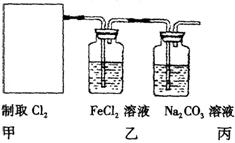
①在该实验中,甲部分的装置是 (填字母);指出a中m仪器的名称 。
②乙装置中FeCl2溶液Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是(填加试剂的名称、至少填二种)方法 、
;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、清毒的物质。已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是 ;
(3)为测定漂白粉中Ca(ClO)2的质量分数,该小组将2.0g漂白粉配制成250mL溶液,取出25mL并向其中依次加入过量稀H2SO4、过量KI溶液,完全反应后,再滴入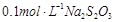 溶液:
溶液: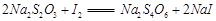 ,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。
,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com