
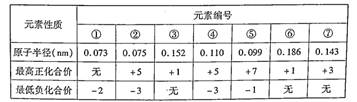
| A.⑦的简单离子不是同周期元素离子半径最小的 |
| B.气态氢化物的稳定性①>② |
| C.②的气态氢化物浓溶液可用于检验氯气管道的泄漏 |
| D.阴离子的还原性④大于⑤,最高价氧化物的水化物的碱性③小于⑥ |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | | a | | b | |
| 3 | c | d | e | f | | g | h | |
| 4 | J | | | | | | k | |



查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素Y的最高价氧化物属于两性氧化物 |
| B.元素M的某种单质可作水处理的消毒剂 |
| C.X、M两种元素形成的化合物中只可能含离子键 |
| D.Y、Z、M三种元素的气态氢化物的热稳定性依次减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔点:CO2<H2O<SiO2<KCl |
| B.粒子半径:K+>Na+>Mg2+>Al3+ |
| C.酸性:H3PO4>H2SO4>HClO4>H2SiO3 |
| D.稳定性:H2O<NH3<PH3<SiH4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.气态氢化物的热稳定性:HnY>HnW |
| B.同周期元素中W的最高价氧化物对应水化物的酸性最强 |
| C.Y和X、Z和X组成的常见化合物中化学键的类型相同 |
| D.原子半径的大小顺序: rW>rZ>rY>rX |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.A能与热水反应产生H2,B 必须与水蒸气反应才产生H2 |
| B.A和B都是元素周期表的主族金属元素,A在 B的左下方 |
| C.1mol A能从酸中置换出1.5molH2,1mol B能从酸中置换出1molH2 |
| D.A和B都是元素周期表的主族金属元素,B的最高价氧化物的水化物不溶于水且具有两性,能被A的最高价氧化物的水化物溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com