
| ʵ�� | ���� | |
| A | ��ȡ������������ | ����ڵ�����ˮ�а��ʵ������μ�FeCl3������Һ������������Һ��ʺ��ɫ��ֹͣ���� |
| B | ϡ��Ũ���� | �Ƚ�Ũ��������ձ��У���������ˮ |
| C | Ũ��ˮ����ʯ�ҷ�Ӧ�Ʊ������NH3 | �������ͨ��Ũ������������ſ������ռ� |
| D | �������������ͱ���̼������Һ | �ӷ�Һ©���Ͽڵ����л��㣬�ٴ��¿ڷų�ˮ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A���Ʊ�������������ʱ����Ҫ��FeCl3������Һ�����ˮ�в����ȣ�
B��Ũ������ܶȴ���ˮ����ϡ�����зų������ȣ�Ӧ�ý�Ũ�������ˮ�У�
C�������ʼ��ԣ��ܹ������ᷴӦ��������Ũ������
D������̼������Һ���²㣬Ӧ���ȴӷ�Һ©���¿ڷų�ˮ�㣬Ȼ���ٵ����л��㣮
��� �⣺A����ȡ������������ķ���Ϊ������ڵ�����ˮ�а��ʵ������μ�FeCl3������Һ������������Һ��ʺ��ɫ��ֹͣ���ȣ���A��ȷ��
B��ϡ��Ũ����ʱ��Ӧ�ý�Ũ�������ˮ�У�˳���ܵߵ�������������Һ�ɽ�����B����
C��Ũ��ˮ����ʯ�ҷ�Ӧ�Ʊ������NH3�����������백����Ӧ��Ӧ���ü�ʯ�Ҹ����C����
D�����������ͱ���̼������Һ�ֲ��Ӧ���ȴӷ�Һ©���¿ڷų�����̼������Һ��Һ��Ȼ��ӷ�Һ©�����Ͽڵ����л��㣬��D����
��ѡA��
���� ���⿼���˻�ѧʵ�鷽�������ۣ���Ŀ�ѶȲ����漰�������������Ʊ������������ʷ������ᴿ��Ũ����ϡ�͵�֪ʶ����ȷ������ѧʵ�������������Ϊ���ؼ�����������������ѧ���Ļ�ѧʵ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ�� Br-��NO3-��Na+��SO32- | |
| B�� | ��ˮ�������C��H+��=1��10 -12 mol•L-1����Һ��K+��Ba2+��HCO3-��Cl- | |
| C�� | 0.1 mol•L-1FeCl3��Һ��K+��NH4+��NO3-��SO42- | |
| D�� | c��H+��/c��OH-��=1��10 -12����Һ��Ca2+��Fe3+��ClO-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
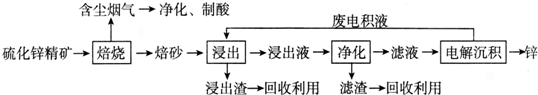
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4��aq�� | B�� | HCl��aq�� | C�� | Fe2��SO4��3��aq�� | D�� | CuSO4��aq�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
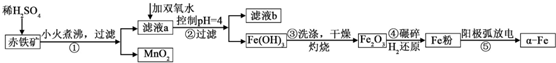
| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��C��=v��D��=0.25mol•L-1•s-1 | B�� | C���������Ϊ28.6% | ||
| C�� | B��ת����Ϊ25% | D�� | z=2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
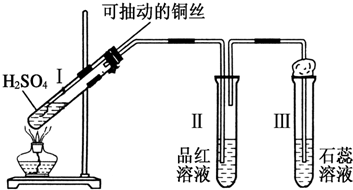
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com