
·ÖĪö Ōµē³ŲÖŠ£¬Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦µÄµē¼«ŹĒøŗ¼«£¬µĆµē×Ó·¢Éś»¹Ō·“Ó¦µÄµē¼«ŹĒÕż¼«£¬µē×Ó“Óøŗ¼«ŃŲµ¼ĻßĮ÷ĻņÕż¼«£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗŌµē³ŲÖŠ£¬Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦µÄµē¼«ŹĒøŗ¼«£¬µĆµē×Ó·¢Éś»¹Ō·“Ó¦µÄµē¼«ŹĒÕż¼«£¬µē×Ó“Óøŗ¼«ŃŲµ¼ĻßĮ÷ĻņÕż¼«£¬øł¾Żµē¼«·“Ó¦Ź½ÖŖ£¬ĶØČėĒāĘųµÄµē¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬ŌņAĪŖøŗ¼«£¬BĪŖÕż¼«£¬µē×Ó“Óøŗ¼«Aµē¼«ŃŲµ¼ĻßĮ÷ĻņÕż¼«Bµē¼«£¬¹Ź“š°øĪŖ£ŗøŗ£»Į÷³ö£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧµēŌ“ŠĀŠĶµē³Ų£¬Ć÷Č·Ōµē³ŲŌĄķŹĒ½ā±¾Ģā¹Ų¼ü£¬ÖŖµĄÕżøŗ¼«µÄÅŠ¶Ļ·½·Ø¼°µē×ÓĮ÷Ļņ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ±øÕ½ÖŠæ¼ŗ®¼ŁĻµĮŠ“š°ø
±øÕ½ÖŠæ¼ŗ®¼ŁĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖ2SO42--2e-ØTS2O82- | |
| B£® | µē½āµÄ×Ü·“Ó¦·½³ĢŹ½ĪŖ2KHSO4$\frac{\underline{\;Ķصē\;}}{\;}$K2S2O8+H2”ü | |
| C£® | Ņ»¶ĪŹ±¼äŗó£¬ČÜŅŗµÄpH¼õŠ” | |
| D£® | µē½ā¹ż³ĢÖŠ£¬Ńō¼«²śÉśĪ¢ĮæÄÜŹ¹ŹŖČóµÄµķ·ŪKIŹŌÖ½±äĄ¶µÄÓŠÉ«µ„ÖŹĘųĢ壬øĆĘųĢåæÉÄÜŹĒO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ąė×Ó¼ü | B£® | ¦Š¼ü | C£® | ÅäĪ»¼ü | D£® | Ēā¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×»ł£ŗ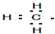 | B£® | CaC2£ŗ | C£® | NH4+£ŗ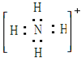 | D£® | ĀČ·Ā£ŗ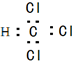 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2SO4 | B£® | MgCl2 | C£® | N2 | D£® | NH4Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com