
| A. | A12O3属于两性氧化物 | |
| B. | 两步反应中CO均是氧化产物 | |
| C. | Al4C3与盐酸反应可生成烃,该烃为乙烯 | |
| D. | 生成的铝粉不能在空气中冷却 |
分析 A.既能与强碱反应又能与酸反应的氧化物是两性氧化物;
B.反应中化合价升高被氧化,生成氧化产物;
C.Al4C3与HCl反应生成AlCl3和另一种物质根据元素守恒判断;
D.Al与氧气能反应生成氧化铝.
解答 解:A.A12O3与强碱反应又能与酸反应,属于两性氧化物,故A正确;
B.两步反应中C元素的化合价均升高被氧化,所以产物CO均是氧化产物,故B正确;
C.Al4C3与HCl反应生成AlCl3,则反应方程式为Al4C3+12HCl=4AlCl3+3CH4↑,所以生成的烃为甲烷,故C错误;
D.Al与氧气能反应生成氧化铝,所以生成的铝粉不能在空气中冷却,故D正确.
故选C.
点评 本题考查了氧化还原反应、两性氧化物、Al的化学性质,题目难度中等,侧重于考查学生的分析能力和应用能力,注意从化合价的角度分析氧化还原反应.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 在氧化还原反应中肯定有一种元素被氧化,另一种元素被还原 | |
| B. | 含有最高价元素的化合物不一定具有很强的氧化性 | |
| C. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| D. | 化合反应和复分解反应不可能是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3 | B. | MgSO4 | C. | CaCl2 | D. | NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4是含氢质量分数最高的有机物 | |
| B. | CH4、CO、H2O均属于共价化合物 | |
| C. | 实验室可用排水法收集CH4、CO、N2 | |
| D. | CO可用HCOOH制取,说明CO是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
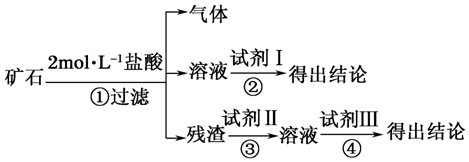
| 编号 | 实验操作 | 预期现象与结论 |
| ① | 取适量矿石研细,加足量2mol•L-1盐酸 | 有大量无色气体产生,得棕黄色溶液,且仍有少量固体残留 |
| ② | ||
| ③ | 取①操作残余固体适量置于烧杯,加入足量2mol•L-1NaOH溶液,充分搅拌 | 残余固体完全溶解于2mol•L-1NaOH溶液,并得无色溶液 |
| ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸钠溶液中加入足量稀硝酸:SO32-+2H-→SO2↑+H2O | |
| B. | 氢氧化钡和硫酸铵两种溶液混合加热:OH-+NH4+$\stackrel{△}{→}$H2O+NH3↑ | |
| C. | 氧化铜溶于稀硫酸中:O2-+2H+→H2O | |
| D. | 硫化氢气体通入氢氧化钠溶液中:H2S+2OH-→2H2O+S2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com