
���� ��1�����ݻ��ϼ۴�����Ϊ0���㣻
��2�����ݹ���������ӹ��ɷ�����
��3���ٵ��ˮ����������������
�ڶ������̴����������Ʊ�������
��4���ٸ���ͬ�ַ���������ͬ��ͬ�������ʲ�ͬ���ǣ�
�ڸ��ݹ���������Һ����ɿ��ǣ�
�۸�������������Ҫ������ˮ���ǣ�
�ܸ���Ӳˮ����ˮ�������ǣ�
��� �⣺��1��������������Ļ��ϼ�Ϊ��1 �ۣ����ݻ������л��ϼ۴�����Ϊ��ԭ��������Ԫ�ػ��ϼ�Ϊ-1���ʴ�Ϊ��-1��
��2���ɻ�ѧʽ����֪����һ������������ӣ�����2��H��2��O��������Ϊ2��1+2��8=18�����������ں�����������������ҲΪ18��
�ʴ�Ϊ��1��1��18��18��
��3���ٵ��ˮ�������������������Է���ʽ�ǣ�2H2O $\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2����
��ʵ�����ö������̴����������Ʊ������ķ�Ӧ���ǹ������⣬��������ˮ������������ʽ�ǣ�2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2�����ʴ�Ϊ��2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
��4����ˮ����������Ȼ���Ԫ��һ�������ǻ�ѧʽ��һ�������Ի�ѧ���ʲ�һ����ͬ�ַ���������ͬ��ͬ�������ʲ�ͬ���ʢٴ���
�ڹ�����������ˮ�����˹���������Һ����Һ��һ�ֻ����ʢڴ���
��ˮ����������Ҫ��������ʣ��ʢ���ȷ��
������ˮʹ����ˮ�����϶����ĭ��Ӳˮ�����϶�ĸ������ʢܴ���
�ʴ�Ϊ���ۣ�
���� �����Թ�������Ϊ���忼��Ԫ���볣��ԭ���ŵĻ��ϼۡ�Ӳˮ����ˮ��������ͻ������б𡢻�ѧ����ʽ����д�ȣ����ڻ���֪ʶ�Ŀ��飬�Ƚϼ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | s��p��d��f���ܼ��Ĺ����Ŀ�ֱ�Ϊ1��3��5��7 | |
| B�� | �����Ӳ���ܼ����Ǵ�s�ܼ���ʼ�� f �ܼ����� | |
| C�� | �����Ӳ㺬�е��ܼ���Ϊ��n-1�� | |
| D�� | �����Ӳ㺬�еĵ�����Ϊ2n2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij��������Һ�У�K+��Fe3+��NO3-��Cl- | |
| B�� | ��0.1mol•L-1 Ba2+����Һ�У�Na+��K+��SO42-��Cl- | |
| C�� | ��0.1mol•L-1 CO32-����Һ�У�OH-��Cl-��NH4+��Na+ | |
| D�� | �������۲���H2����Һ�У�Al3+��Na+��SO42-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4��Ħ������Ϊ16g | |
| B�� | ��״���£�18 g H2O�������22.4 L | |
| C�� | 17 g NH3�����ʵ�����1 mol | |
| D�� | �����ӵ�����ԼΪ6.02��1023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�������ˮ�ܵ����H+��Cl-�������Ȼ��������ӻ����� | |
| B�� | �⾧������ת��ɵ����������յ��������ڿ˷���ԭ��֮��������� | |
| C�� | �ռ��������ˮ�Ĺ����У����ۼ����ƻ� | |
| D�� | �л�������CH3CH2NO2��H2N-CH2-COOH��ͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �á�84����Һ���������� | |
| B�� | ��Ũ������������������ | |
| C�� | �û���̿������װ��������к����� | |
| D�� | ��С�մ�����θ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
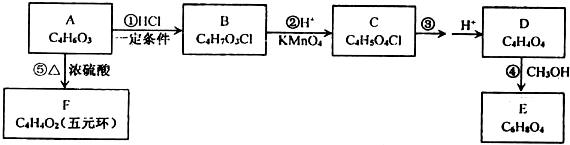
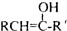 ��R�� R�䣬��������� H�����ȶ�����������ʾ������Ǵ���ṹ��
��R�� R�䣬��������� H�����ȶ�����������ʾ������Ǵ���ṹ�� 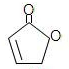 E����ʽ����
E����ʽ����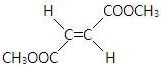
 ��
��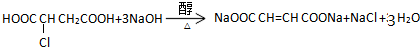 ��
�� ��
��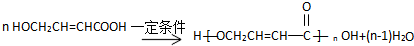 ��
��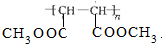 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com