
【题目】下列说法正确的是( )
A. 易溶于水的物质一定是电解质
B. 液态氯化氢能导电
C. 液态氯化钠能导电
D. 熔融状态的钠是电解质
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁.“速力菲”是市场上一种常见的补铁药物,如图1是它的说明书: 
该药品中Fe2+会缓慢氧化,国家规定该药物中Fe2+的氧化率超过10%即不能再服用.
(1)为了检验某药店出售的“速力菲”是否被氧化,实验室可选用的最常用且最灵敏的检验试剂为(填试剂的名称).
(2)实验室采用H2SO4酸化的KMnO4溶液对“速力菲”中的Fe2+进行滴定(假设药品中其他成分不与KMnO4反应);该反应的离子方程式为: .
(3)称量上述含铁元素质量分数为20.00%的“速力菲”19.00g,将其全部溶于稀硫酸中,配制成1000.00mL溶液.取出20.00mL,用0.01300mol/L的KMnO4溶液滴定,消耗KMnO4溶液体积如图2所示.
①实验前,首先要精确配制0.01300mol/L KMnO4溶液250mL,配制时需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需 .
②某同学的滴定方式(夹持部分略去)如图,最合理的是 . 
③由图可知消耗KMnO4溶液体积为mL;
④滴定终点观察到的现象为;
⑤以标准KMnO4溶液滴定样品溶液的浓度,判断以下操作所引起实验结果偏小的是 .
A.滴定过程中,锥形瓶振荡太剧烈,有少量液滴溅出
B.未用标准KMnO4溶液润洗滴定管
C.滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁
D.滴定前仰视,滴定后俯视(标准液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 在共价化合物中一定含有共价键
B. 含有离子键的化合物一定是离子化合物
C. 含有共价键的化合物一定是共价化合物
D. 化学反应过程中,反应物分子内的化学键断裂,产物分子的化学键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500℃,在三个相同体积的恒容密闭容器里,分别加入对应物质,甲:2mol SO2 1mol O2乙:2mol SO2 1mol O2 1mol N2 丙:4mol SO2 2mol O2同时进行反应,开始时反应速率最大的是( )
A.甲
B.乙
C.丙
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.![]() =1012的溶液中:K+、NH4+、SO42﹣、NO3﹣
=1012的溶液中:K+、NH4+、SO42﹣、NO3﹣
B.0.1 mol/L NaAlO2溶液:Fe3+、H+、Cl﹣、SO42﹣
C.与铝反应产生大量气体的溶液:Na+、K+、CO32﹣、NO3﹣
D.使甲基橙试液显黄色的溶液:Fe2+、Mg2+、NO3﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJmol﹣1)P﹣P:198 P﹣O:360 O═O:498则反应P4(白磷)+3O2→P4O6的能量变化为( ) 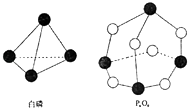
A.释放1638kJ的能量
B.吸收1638kJ的能量
C.释放126kJ的能量
D.吸收126kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究物质的性质具有重要意义.请回答下列问题:
(1)请配平以下化学方程式:
Al+NaNO3+NaOH=NaAlO2+N2↑+H2O
若反应过程中转移5mol电子,则生成标准状况下N2的体积为L.
(2)25℃时,将a molL﹣1的氨水与0.1molL﹣1的盐酸等体积混合,当溶液中离子浓度关系满足c(NH4+)>c(Cl﹣)时,则反应的情况可能为 .
a.盐酸不足,氨水剩余b.氨水与盐酸恰好完全反应c.盐酸过量
(3)向NH4HSO4溶液中滴加少量的Ba(OH)2溶液的离子方程式 .
(4)25℃,两种酸的电离平衡常数如表.
Ka1 | Ka2 | |
H2SO3 | 1.3×10﹣2 | 6.3×10﹣8 |
H2CO3 | 4.2×10﹣7 | 5.6×10﹣11 |
①HSO3﹣的电离平衡常数表达式K= .
②0.10molL﹣1Na2SO3溶液中离子浓度由大到小的顺序为 .
③H2SO3溶液和NaHCO3溶液混合,主要反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经测定一瓶气体中只含C和O两种元素,通常情况下这瓶气体不可能是( )
A. 一种化合物B. 两种单质
C. 两种化合物D. 一种单质和一种化合物的混合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com