
分析 n(混合气体)=$\frac{11.2L}{22.4L/mol}$=0.5mol,设CO和CO2的物质的量分别为x、y,
则$\left\{\begin{array}{l}{x+y=0.5}\\{28x+44y=18.8}\end{array}\right.$,结合ρ=$\frac{m}{V}$计算;
解答 解:(1)n(混合气体)=$\frac{11.2L}{22.4L/mol}$=0.5mol,设CO和CO2的物质的量分别为x、y,
则$\left\{\begin{array}{l}{x+y=0.5}\\{28x+44y=18.8}\end{array}\right.$,解得x=0.2mol,y=0.3mol,
n(CO):n(CO2)=0.2mol:0.3mol=2:3,
CO的物质的量的分数为$\frac{0.2mol×28g/mol}{18.8g}$×100%=40%,CO2的质量分数为$\frac{0.3mol×44g/mol}{18.8g}×100%$=70.2%;
由ρ=$\frac{m}{V}$可知,气体的密度为$\frac{18.8g}{11.2L}$=1.68g/L,
故答案为:2:3;40%;70.2%;1.68.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的量、体积的关系为解答的关键,注重基本公式及计算能力的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
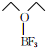 )的熔点为-58℃,沸点为126~129℃,它属于分子晶体.
)的熔点为-58℃,沸点为126~129℃,它属于分子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
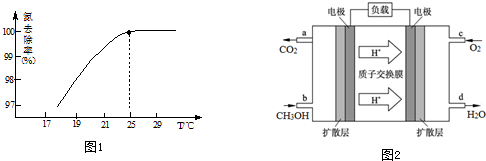
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取氯乙烷(CH3一CH2Cl)的最好的方法是乙烷与氯气发生取代反应 | |
| B. | 乙烯、苯都能使溴水褪色,两者的褪色原理相同 | |
| C. | 2-丁烯不存在顺反异构体 | |
| D. | 研究有机物一般要经过的基本步骤为:分离、提纯→元素定量分析(确定实验式)→测定相对分子质量(确定分子式)→波谱分析(确定结构式),其中最早提出元素定量分析的是法国化学家李比希 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a×b×18×6.02×1023 | B. | $\frac{18b}{a}$×6.02×1023 | ||
| C. | $\frac{18a}{b}$×6.02×1023 | D. | $\frac{b}{18a}$×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应既属于氧化还原反应,又属于离子反应 | |
| B. | 生成1 mol Cl2转移电子数均为2NA | |
| C. | 盐酸浓度越大,Cl-的还原性越强 | |
| D. | 氧化性:KMnO4>K2Cr2O7>Cl2>MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液中水电离出的c(H+)=10-10 mol•L-1 | |
| B. | 溶液中c(H+)+c(A-)=0.1 mol•L-1 | |
| C. | 与0.05 mol•L-1 NaOH溶液等体积混合,水的电离平衡向正向移动 | |
| D. | 上述溶液中加入一定量NaA晶体或加水稀释,溶液的c(OH-)均增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com