
下列对一些实验事实的理论解释正确的是( )
选项 | 实验事实 | 理论解释 |
A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
B | CO2为直线形分子 | CO2分子中C===O之间的夹角为180° |
C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
科目:高中化学 来源:2016届福建省高三下学期周考五理科综合化学试卷(解析版) 题型:填空题
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:
Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1,
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为__________。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:__________。
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g) 测得CH3OH的物质的量随时间的变化见图1。
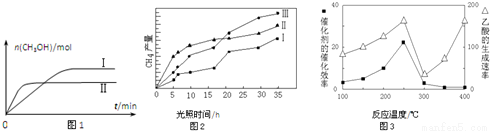
①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ__________KⅡ(填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容 器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为__________。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化见图2.在0~15小时内,CH4的平均生成速率I、II和III从大到小的顺序为__________(填序号).
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3。
①乙酸的生成速率主要取决于温度影响的范围是__________。
②Cu2Al2O4可溶于稀硝酸,写出有关的离子方程式:__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁鞍山一中高二下期中化学试卷(解析版) 题型:选择题
正硼酸(H3BO3)是一种层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如下图),下列有关说法正确的是( )
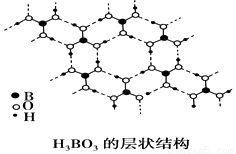
A.正硼酸晶体属于原子晶体
B.H3BO3分子的稳定性与氢键有关
C.分子中硼原子最外层满足8电子稳定结构
D.1 mol H3BO3晶体中有3 mol氢键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
填写下列空白
(1)第三周期原子半径最小的元素__________。
(2)含有8个质子,10个中子的原子的化学符号__________。
(3)最外层电子排布为4s24p1的原子的核电荷数为__________。
(4)周期表中最活泼的非金属元素价电子排布图为__________。
(5)下列物质中,只含有极性键的分子是 ,既含离子键又含共价键的化合物是 ;只存在σ键的分子是 ,同时存在σ键和π键的分子是 。
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
下列说法中,正确的是( )
A.冰融化时,分子中H—O键发生断裂
B.原子晶体中,共价键的键长越短,通常熔点就越高
C.分子晶体中,共价键键能越大,该晶体的熔、沸点就越高
D.分子晶体中,分子间作用力越大,则分子越稳定
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中文科化学试卷(解析版) 题型:计算题
在一定条件下,发生如下反应:N2 +3H2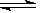 2NH3,5s内N2的浓度增加了0.025mol/L,H2的浓度增加了0.075mol/L,NH3的浓度增加了0.050mol/L,则用N2、 H2、NH3的浓度变化表示的速率分别为v(N2)= mol/(L•s) ,v(H2)= mol/(L•s) ,v(NH3) mol/(L•s),v(N2)∶v(H2)∶v(NH3)=_______________________
2NH3,5s内N2的浓度增加了0.025mol/L,H2的浓度增加了0.075mol/L,NH3的浓度增加了0.050mol/L,则用N2、 H2、NH3的浓度变化表示的速率分别为v(N2)= mol/(L•s) ,v(H2)= mol/(L•s) ,v(NH3) mol/(L•s),v(N2)∶v(H2)∶v(NH3)=_______________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中文科化学试卷(解析版) 题型:选择题
甲、乙两个容器内都进行A→B的反应,甲容器内每分钟减少了4 mol A,乙容器内每分钟减少2 molA,则甲容器内的反应速率比乙容器内的反应速率( )
A.快 B.慢 C.相等 D.无法判断
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中理科化学试卷(解析版) 题型:选择题
微型钮扣电池在现代生活中有广泛的应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液是KOH,电极反应式为Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-。总反应式是Ag2O+Zn===2Ag+ZnO。根据上述反应式,判断下列叙述中正确的是 ( )
A.在使用的过程中,电池正极区溶液的pH减小
B.在使用的过程中,电子由Ag2O极经外电路流向Zn极
C.Zn极是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建师大附中高一下期中化学试卷(解析版) 题型:选择题
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量B跟Cl2反应除生成C外,另一产物是盐酸盐。
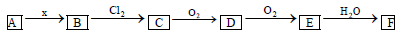
下列说法不正确的是( )
A.当X是强酸时,A、B、C、D、E、F均含同一种元素,F是H2SO4
B.当X是强碱时,A、B、C、D、E、F均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C常温下是气态单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com