
【题目】(1)根据要求回答下列问题:
①干冰与CO2;②白磷与红磷;③![]() Cl与
Cl与![]() Cl;④液氯与氯水;⑤
Cl;④液氯与氯水;⑤![]() 与
与 。在上述各组物质中:
。在上述各组物质中:
互为同位素的是__________________;
互为同素异形体的是__________________;
互为同分异构体的是__________________;
属于同种物质的是__________________。(填序号,下同)
(2)现有以下六种物质形成的晶体:a.NH4Cl;b.SiO2;c.Na2O2;d.干冰;e.C60;f.Ne请用相应字母填空:
属于分子晶体的是__________________;属于共价化合物的是__________________;属于离子化合物的是___________;熔化时只需要破坏共价键的是__________________;既含有离子键又含有非极性共价键的是__________________;不存在化学键的是__________________。
【答案】③ ② ⑤ ① def bd ac b c f
【解析】
(1)根据同一物质分子式和结构相同、同位素是质子数相同而中子数不同的原子、同素异形体是由同一元素组成的不同性质的单质、同分异构体是分子式相同而结构不同的化合物分析判断;
(2)分子晶体的构成微粒是分子,作用力是分子间作用力;共价化合物是原子之间以共价键形成的化合物;原子晶体构成微粒是原子,作用力是共价键;离子晶体是阴阳离子之间以离子键结合形成的化合物,若阴离子或阳离子为复杂离子,则还含有共价键;若物质构成微粒是单原子分子,则物质内不含有化学键。
(1)①干冰是固态CO2,因此干冰与CO2属于同一物质;
②白磷与红磷是由P元素组成的不同性质的单质,二者互为同素异形体;
③3517Cl与3717Cl质子数都是17,中子数分别是18、20,二者互为同位素;
④液氯是液态Cl2,属于纯净物,而氯水是氯气的水溶液,其中含有Cl2、HCl、HClO、H2O等多种组分,属于混合物;
⑤![]() 名称为2,3-二甲基丁烷,分子式为C6H14,
名称为2,3-二甲基丁烷,分子式为C6H14,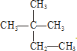 名称为2,2-二甲基丁烷,分子式为C6H14,二者分子式相同,结构不同,互为同分异构体。
名称为2,2-二甲基丁烷,分子式为C6H14,二者分子式相同,结构不同,互为同分异构体。
故在上述各组物质中,互为同位素的序号是③;互为同素异形体序号是②;互为同分异构体的序号是⑤;属于同种物质的序号是①
(2) a.NH4Cl由NH4+与Cl-之间通过离子键结合形成离子晶体,在阳离子NH4+中含有共价键,因此NH4Cl中含有离子键、共价键;
b.SiO2是由Si原子与O原子通过共价键形成的原子晶体,构成微粒是原子,作用力为共价键,属于共价化合物;
c.Na2O2是由Na+与O22-之间通过离子键结合形成的离子化合物,在O22-中含有非极性共价键,因此其中含有的化学键为离子键、共价键;
d.干冰是固体CO2,是由CO2分子通过分子间作用力结合形成的分子晶体,在分子内含有共价键,属于共价化合物;
e.C60是由分子通过分子间作用力形成的分子晶体,分子内C原子之间以共价键结合,由于只含有C元素,属于单质;
f.Ne是由分子通过分子间作用力构成的分子晶体,一个Ne原子就是一个分子,不存在化学键。
故在上述物质中,属于分子晶体的序号是def;属于共价化合物的序号是bd;属于离子化合物的是ac;熔化时只需要破坏共价键的序号是b;既含有离子键又含有非极性共价键的是c;不存在化学键的是f。


科目:高中化学 来源: 题型:
【题目】一种肼(N2H4)燃料电池的结构如图所示,下列说法正确的是 ( )
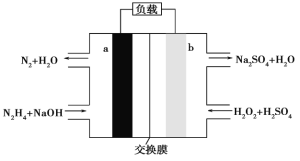
A.a为正极,电极反应式为:N2H4-4e-+4OH-=N2↑+4H2O
B.外电路中每通过1mol 电子,则有NA个Na+穿过交换膜向正极移动
C.b极的电极反应式为H2O2+2e-=2OH-
D.用该电池作电源电解饱和食盐水,当得到0.1mol Cl2时,至少要消耗0.1mol N2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲为恒压容器、乙为恒容容器。相同条件下充入等物质的量的![]() 气体,且起始时体积相同。发生反应:
气体,且起始时体积相同。发生反应:![]() .一段时间后相继达到平衡状态下列说法中正确的是( )
.一段时间后相继达到平衡状态下列说法中正确的是( )
甲 乙
乙
A.平衡时![]() 体积分数:甲<乙
体积分数:甲<乙
B.达到平衡所需时间,甲与乙相等
C.该反应的平衡常数表达式![]() )
)
D.若两容器内气体的压强保持不变,均说明反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)实验室利用如图装置进行中和热的测定。回答下列问题:
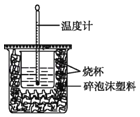
(1)该图中有一处未画出,它是_____(填仪器名称)。
(2)如果用0.50 mol/L的盐酸和氢氧化钠固体进行实验,则根据此实验的数据书写中和热的热化学方程式中的△H将_____(填“偏大”“偏小”或“不变”),原因是_____。
(3)利用50 mL 0.50 mol/L的稀盐酸与50 mL 0.55 mol/L的稀氢氧化钠溶液进行实验,设溶液的密度均为1 g/cm3,中和后溶液的比热容c=4.18 J/(g℃),请根据实验数据计算,中和热△H=_____ (取小数点后一位)。
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
盐酸 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.4 |
2 | 27.0 | 27.4 | 27.2 | 31.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
(4)上述(3)中的结果与中和热的理论值有偏差,产生偏差的原因可能是_____
a.实验装置保温、隔热效果差
b.使用环形玻璃搅拌棒搅拌,使其充分反应
c.分多次把NaOH溶液倒入盛有稀盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度
(二)某学生用0.2000molL﹣1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固体好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答:
(1)以上步骤有错误的是(填编号)_____,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)_____。
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无影响”)_____。
(3)判断滴定终点的现象是:_____。
(4)如图是某次滴定时的滴定管中的液面,其读数为_____mL。

(5)根据下列数据:请计算待测盐酸溶液的浓度:_____。
滴定次数 | 待测体积(mL) | 标准烧碱体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 20.00 | 0.30 | 20.40 |
第二次 | 20.00 | 4.00 | 24.20 |
第三次 | 20.00 | 2.00 | 24.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.v(A)=0.5mol/(L·min)B.v(D)=1mol/(L·min)
C.v(C)=0.8mol/(L·min)D.v(B)=0.3mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)![]() 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是
A. 550℃时,若充入惰性气体,正,逆 均减小,平衡不移动
B. 650℃时,反应达平衡后CO2的转化率为25.0%
C. T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D. 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0P总
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是无色透明有刺激性气味的液体,制备的实验装置如图所示。下列说法不正确的是( )

A.先在试管a中加入乙醇,然后边振荡试管边缓慢加入浓硫酸和乙酸
B.浓硫酸的作用主要是催化和吸水
C.b中的饱和Na2CO3溶液可用浓NaOH溶液代替
D.实验原理为CH3COOH+H18OC2H5![]() CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00 mL浓度均为 0.10mol L-1的CH3COOH(Ka=1.75×10-5)溶液和HCN (Ka=4.9×10-10)溶液所得滴定曲线如图。下列说法正确的是

A. 曲线I和曲线Ⅱ分别代表的是CH3COOH和HCN
B. 点③和点⑤所示溶液中:c(CN-)=c(CH3COO-)
C. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D. 在点②和③之间(不包括端点)存在关系: c(Na+)>c(A-)>c(H+)>c(OH-) (A-代表溶液中的酸根离子)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)在室温下,等体积、等浓度的氢氧化钠与醋酸混合后溶液呈__性,溶液中c(Na+)__c(CH3COO-)(填“>”“=”或“<”);pH=13的氢氧化钠与pH=1的醋酸等体积混合后溶液呈__性,溶液中c(Na+)___c(CH3COO-)(填“>”“=”或“<”);
(2)下列溶液,①0.1mol/L HCl溶液②0.1mol/L H2SO4溶液③0.1mol/L NaOH溶液④0.1mol/L CH3COOH溶液,按pH由小到大顺序为___。
(3)CuSO4的水溶液呈酸性的原因是(用离子方程式表示):____;实验室在配制CuSO4的溶液时,常将CuSO4固体先溶于较浓的硫酸中,然后再用蒸馏水稀释到所需的浓度,以___(填“促进”、“抑制”)其水解。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,充分反应后溶液呈中性,则反应后溶液存在的离子有____,其浓度由大到小的顺序为_____,氨水的浓度a__0.01 mol·L-1(填“>”、“ <”或“=”)。
(5)已知:难溶电解质Cu(OH)2在常温下的KSP=2×10-20,则常温下:某CuSO4溶液中c(Cu2+)=0.02molL-1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为____。
(6)某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:


①酸浸后加入H2O2的目的是_____________,调pH的最适宜范围为_______。
②调pH过程中加入的试剂最好是_________。
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
③煮沸CuSO4溶液的原因是_____;向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,反应的化学方程式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com