
| �¶�/�� | 800 | 1000 | 1200 | 1400 |
| ƽ�ⳣ�� | 0.45 | 1.92 | 276.5 | 1771.5 |
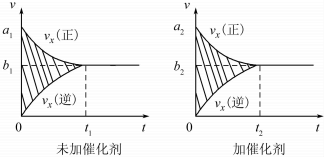
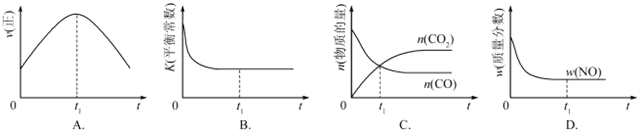
���� ��1���ټ�����������淴Ӧ���ʶ����ﵽƽ������ʱ����٣���ƽ�ⲻ�ƶ���
��A������ƽ���������������ȣ����ٱ仯��
B������ƽ����¶�Ϊ��ֵ��ƽ�ⳣ�����䣬��Ϸ�Ӧ���ж��淴Ӧ�����������¶ȱ仯���ж��¶ȶԻ�ѧƽ�ⳣ����Ӱ�죻
C��t1ʱ�̺������̼��CO�����ʵ��������仯������ٱ仯��
D������ƽ������ֵĺ����������仯��
��2�����ݸ�˹���ɣ�����֪�Ȼ�ѧ����ʽ�����ʵ���ϵ�����мӼ�����Ŀ���Ȼ�ѧ����ʽ��
��3�����¶����ߣ�ƽ�ⳣ������ƽ��������Ӧ�����ƶ���
��T��ʱ����1L�ܱ�������Ͷ��1molCH4��1mol H2O��g����ƽ��ʱc��CH4��=0.5mol•L-1������ƽ��Ũ�ȣ����ƽ�ⳣ���ı���ʽ���㣻
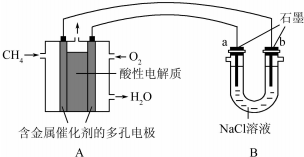
��4����ԭ��ظ�������������Ӧ�������ڸ���ͨ�룬���������£�����������Ӧ����CO2��H+��
�ڸ��ݵ���Ȼ�����Һ�ĵ�ⷽ��ʽ������Һ��PH��
�۵������У�����������������֮����ˮ�������������������������������ʵ����ж�������������������ʵ�����Ȼ����������µ�������������������
��� �⣺��1���ټ�����������淴Ӧ���ʶ����ﵽƽ������ʱ����٣���ƽ�ⲻ�ƶ�����ͼ����Ӱ����������䣬�ʴ�Ϊ��BC��
��A������ƽ���������������ȣ����ٱ仯��t1ʱ��V�����֮���淴Ӧ�������ʷ����仯��δ����ƽ�⣬��A����
B���÷�Ӧ����ӦΪ���ȷ�Ӧ���淴Ӧ�����¶����ߣ���ѧƽ�ⳣ����С������ƽ����¶�Ϊ��ֵ������ߣ�ƽ�ⳣ�����䣬Ϊ��С��ͼ����ʵ�ʷ��ϣ���B��ȷ��
C��t1ʱ�̺������̼��CO�����ʵ��������仯��t1ʱ��δ����ƽ��״̬����C����
D��NO����������Ϊ��ֵ��t1ʱ�̴���ƽ��״̬����D��ȷ��
�ʴ�Ϊ��BD��
��2����֪��CH4��g��+2NO2��g���TN2��g��+CO2��g��+2H2O��g����H1=-867kJ/mol��
2NO2��g��?N2O4��g����H2=-56.9kJ/mol��
H2O��g��=H2O��l����H=-44.0kJ/mol��
���ݸ�˹���ɣ���-��+�ܡ�2�ɵ�CH4��g��+N2O4��g��=N2��g��+CO2��g��+2H2O��l�����ʡ�H=-867kJ/mol-��-56.9kJ/mol��+2��-44.0��kJ/mol=-898.1kJ/mol ��CH4��g��+N2O4��g���TN2��g��+2H2O��l��+CO2��g����H=-898.1kJ/mol��
�ʴ�Ϊ��CH4��g��+N2O4��g���TN2��g��+2H2O��l��+CO2��g����H=-898.1kJ/mol��
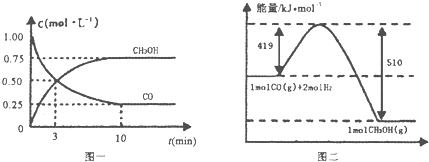
��3�����¶����ߣ�ƽ�ⳣ������ƽ��������Ӧ�����ƶ����ʸ÷�ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
��T��ʱ����1L�ܱ�������Ͷ��1molCH4��1mol H2O��g����ƽ��ʱc��CH4��=0.5mol•L-1�����¶�K=$\frac{c��CO��•{c}^{3}��{H}_{2}��}{c��C{H}_{4}��•c��{H}_{2}O��}$=$\frac{0.5��1��{5}^{3}}{0.5��0.5}$=6.75��
�ʴ�Ϊ��6.75��
��4���١�ԭ��ظ�������������Ӧ�������ڸ���ͨ�룬���������£�����������Ӧ����CO2��H+�������缫��ӦʽΪ��CH4-8e-+2H2O=CO2+8H+��
�ʴ�Ϊ��CH4-8e-+2H2O=CO2+8H+��
��100mL 1mol/Lʳ��ˮ�к����Ȼ���0.1mol�����ݷ�Ӧ����ʽ2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+H2��+Cl2����֪�����0.1molNaCl����0.1mol�������ƺ�0.05mol������ͬʱ����0.05mol�������������ʵ��Ϊ���ˮ�������2.24L���������ʵ���Ϊ0.1mol�����ˮ����0.05mol����������0.025mol���������������������ܹ�����0.075mol���壬
������ɱ����2.24L����ʱ��NaCl��ȫ��⣬����0.1molNaOH����Һ���Ϊ0.1L����c��OH-��=1mol/L��c��H+��=10-14������PH=14��
�ʴ�Ϊ��14��
�۸��ݢڵķ�����֪��������������������0.05mol������0.025mol�������ܹ�����0.075mol���壬��״��������������������Ϊ��22.4L/mol��0.075mol=1.68L��
�ʴ�Ϊ��1.68��
���� ���⿼���˻�ѧƽ�ⳣ��Ӱ�����ؼ����㡢���ԭ�����Ȼ�ѧ����ʽ����д��֪ʶ����Ŀ�ѶȽϴ������漰��֪ʶ��϶࣬���������ѧ���ķ�����������������ѧ����������ע�����ջ�ѧƽ�ⳣ���ĸ������ʽ����Ӱ�����أ���ȷ���ԭ�����ܹ���ȷ��д�缫��Ӧʽ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ȼҵ�ǵ�����ڵ�NaCl����������Cl2 | |
| B�� | ����ȼ�ϵ�ؿɽ�����ֱ��ת��Ϊ���� | |
| C�� | ԭ��ع���ʱ�����ӴӸ��������·�������� | |
| D�� | ��ҵ�ϵ�����ڵ�AlCl3����ȡ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������м���Ũ�������ַ�������˵��Ũ���������ˮ�� | |
| B�� | Ũ�����ڹ�������ɫ��ƣ�˵��Ũ����ȶ� | |
| C�� | �����£�Ũ����������������棬˵������Ũ�����Ӧ | |
| D�� | ���ˮ�еμ�CCl4�����ú�ֲ㣬CCl4����Ϻ�ɫ��˵������CCl4�ӵ�ˮ����ȡ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ��Ӧ��Ͷ����� | ��Ӧ���ת���� | CH3OH��Ũ�� | �����仯 ��Q1��Q2��Q3������0�� |
| �� | 1mol CO��2mol H2 | a1 | c1 | �ų�Q1kJ���� |
| �� | 1mol CH3OH | a2 | c2 | ����Q2kJ���� |
| �� | 2mol CO��4mol H2 | a3 | c3 | �ų�Q3kJ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
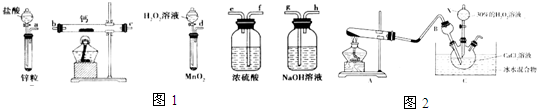
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
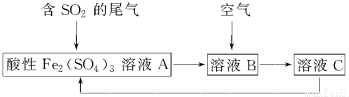
| A�� | ��ҺB�з����ķ�ӦΪ2SO2+O2�T2SO3 | |
| B�� | �������Ը��������Һ������ҺC���Ƿ���Fe3+ | |
| C�� | ���������̿���֪�����ԣ�Fe3+��O2��SO42- | |
| D�� | �˹��յ��ŵ�֮һ��������ѭ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ͭ�������л���ʱ��Ҳ����ֹ�������� | |
| B�� | �ڿ����н���������Ѹ�ٱ������γɱ���Ĥ | |
| C�� | ��˿��Ũ�����ڳ����¶ۻ� | |
| D�� | ������ϡH2SO4��Ӧʱ���Ӽ���CuSO4��Һ���ɼӿ�H2�IJ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ�ӵ��������ǵ������ԭ������ | |
| B�� | ������Ħ��������8g•mol-1 | |
| C�� | 1molH2SO4�к�1molH2 | |
| D�� | 1molH2O��������18g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
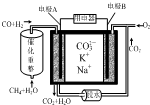
| A�� | �缫AΪ�����������˻�ԭ��Ӧ | |
| B�� | �缫A��CO����ĵ缫��ӦΪ��CO+O2--2e-�TCO2 | |
| C�� | �缫B�Ϸ����ĵ缫��ӦΪ��O2+2CO2+4e-�T2CO32- | |
| D�� | ��ع���ʱ��K+��缫A�ƶ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com