
A,B,C,D均为主族元素,最外层电子数分别为1,4,6,7,原子序数大小为D<B<A<C。 C元素的一种同位素原子核中有46个中子,它的气态氢化物的相对分子质量与最高价氧化物的相对分子质量之比为1:1.56。
(1) 通过计算,确定C元素所在周期及族。
(2) A,B,D是什么元素?
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源:广东省2009届高三化学各地名校月考试题汇编-无机化学综合 题型:058
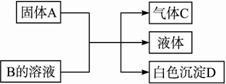
A、B、C、D均为中学化学常见的物质,其组成元素均为主族元素.它们间的反应关系如图所示.
(1)若A为金属钠,B为饱和Ca(OH)2溶液,则白色沉淀D为________(写化学式)
(2)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则A与B反应(可加热)的离子方程式为:____________________________.
(3)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液,A的相对分子质量与D相同.向一定量的B溶液中逐渐加入固体粉末A,当A与B以物质的量之比3∶1反应时,生成的D的量最多.推知A的化学式为________,B的化学式为________,D与NaOH溶液反应的离子方程式是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
A.ABCD B.CDBA? C.ABDC D.DCAB
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)若A为金属钠,B为饱和NaOH溶液,则白色沉淀D为 (写化学式)。?
(2)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则A与B反应(可加热)的化学方程式为 。?
(3)若A是碳化钙(CaC2),B是一种盐,A与B的溶液反应时只生成气体C、CaCO3和水;则B的化学式为 ;若C的燃烧热为1 300 kJ·mol-1,则C燃烧的热化学方程式为 。?
(4)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液,A的相对分子质量与D相同,向一定量的B溶液中逐渐加入固体粉末A,当A与B以物质的量之比3∶1反应时,生成的D的量最多。推知A的化学式为 ,B的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com