
����Ŀ��ij���������Ҫ�ɷ�ΪAl2O3��xH2O��������Fe2O3��SiO2���ʡ���ȡ17.5g��������Ʒ������200mL1.65mol/LϡH2SO4��ǡ����ȫ��Ӧ�����˵õ�����0.3g��Ȼ������Һ�м�������NaOH��Һ���õ�����2.14g������ʾ��SiO2���ʲ���ϡ���ᷴӦ��
��1�������Ʒ��Fe2O3�����ʵ�����____��
��2���Լ�����Ʒ��Al2O3��������____��
��3���Լ�����Ʒ��Al2O3��xH2O��xֵ��____��
���𰸡�0.01mol 10.2g 3
��������
�������������������ᷴӦ�����������費��Ӧ����0.3gΪ�����������������Һ�м����������������ƣ�������ת��Ϊƫ�����Σ��ʵõ�����2.14gΪ����������������
��1������FeԪ���غ㣬n��Fe2O3��=![]() nFe(OH)3=
nFe(OH)3=![]() ��
��![]() =0.01mol��
=0.01mol��
����0.01mol��
��2������������غ㣺3n[Al2(SO4)3]+3n[Fe2(SO4)3]=n(H2SO4)����3n[Al2(SO4)3]+3��0.01mol
=0.2L��1.65mol/L����n[Al2(SO4)3]=0.1mol������AlԪ���غ㣬n��Al2O3��=n[Al2��SO4��3]=0.1mol����m��Al2O3��=0.1mol��102g/mol=10.2g��
����10.2g��
��4����Ʒ��ˮ������Ϊ17.5g-0.3g-10.2g-0.01mol��160g/mol=5.4g�����ʵ���Ϊ![]() =0.3mol����0.1mol��0.3mol=1��x����x=3��
=0.3mol����0.1mol��0.3mol=1��x����x=3��
����3��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��鶼Ϊ���ֻ���������ˮʱ����������ӣ���Na����OH����![]() ����H����Cl����
����H����Cl����![]() ����Na����K����OH������Na����K����
����Na����K����OH������Na����K����![]() �����а��ս����ᡢ������ε������(����)
�����а��ս����ᡢ������ε������(����)
A. �ڢۢ� B. �ڢ٢�
C. �ڢۢ� D. �ڢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�ͼ���ܽϳ�ʱ�俴��������������ɫ�������ǣ� ��


A. �٢ڢۢܢ�B. �٢ڢ�C. �٢ڢۢ�D. �ڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������壨FeSO4��7H2O����ҽҩ������Ѫ����ij����С��ⶨ�ò�Ѫ������Ԫ�صĺ�����������ò�Ѫ���Ƿ���ʡ�ʵ�鲽�����£�

��ش��������⣺
��1��������ٵ���Һ�еμ�KSCN��Һ���Ϊ��ɫ�������Һ�к���______�������ӷ��ţ���
��2���������з�Ӧ�����ӷ���ʽ��__________________________________��
��3���������з�Ӧ�����ӷ���ʽ��__________________________________��
��4����������һϵ�д����IJ������裺���ˡ�______�����ա�_______��������
��5������ʵ���е���ĺ��Բ��ƣ���ÿƬ��Ѫ������Ԫ�ص�����Ϊ______g�����ú�a�Ĵ���ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij̽��ѧϰС����һ�������Ҵ����Ʒ�Ӧ�Ʋ��Ҵ��ṹ��ʵ��װ��ͼ��ͼ��ʾ.����ʵ�������������������
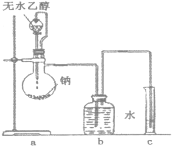
A.ʵ��ʱӦ��֤�Ҵ����������Ʒ�Ӧ��ȫ
B.װ��b�н������ܲ�Ӧ����ˮ�У���ˮ����Ӧ�嵽����ƿ�ײ�
C.ͨ���ⶨ�ų������������������Ҵ��л��������Ŀ���Ӷ��Ʋ��Ҵ��Ľṹ
D.����Ͳ�ж�ȡ�ų���ˮ�����ʱ��Ӧע�������ƶ���Ͳʹ��Ͳ�ڵ�Һ���뼯��ƿ�е�Һ����ƽ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���������ϴ�����ͼ��ϵ�������и����˵����ȷ���ǣ�������

A. �����������������ڽ����ϵ
B. ������ǵ�������ڰ�����ϵ
C. ��Һ���ɢϵ���ڲ��й�ϵ
D. ���������������ڰ�����ϵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������ܷ�����Ӧ��ij��ȤС��Դ˽���̽������������ּ��衣
����һ��Na2O2��2NO2===2NaNO2��O2��
�������Na2O2��2NO2===2NaNO3
[��������]
2NaNO2��2HCl===2NaCl��NO����NO2����H2O
2NO2��2NaOH===NaNO2��NaNO3��H2O
[ʵ��̽��]
��.��ͼʾװ�ý���ʵ�顣

��.ͨ������������������Ʒ�Ӧ��ȫ��Ȼ��Բ������еĹ������ʽ��м��顣
[ʵ�����]��ʵ�������������������������������������Ӧ��
(1)������������������ķ�Ӧ�У���������____��
(2)װ��A�з�Ӧ�����ӷ���ʽ��________��
(3)װ��C��������__________��
(4)�����ʵ��֤��װ��B�еķ�Ӧ������������һ����
��ʵ�������ȡ�������еĹ��������Թ��У�________��
��ʵ��������________��
(5)��ͬѧ��Ϊ��ֻҪֱ�ӹ۲�C�е��ܿ��Ƿ�������ð�����Ϳ����ж�B�еķ�Ӧ������һ�ּ��裬�����뷨________(������������������)��ԭ����___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼ�ת���Ŀ�ͼ���ش��й����⣺

(1)д����ͼ������A��B��E��F�ֱ�ָ�����ʵĻ�ѧʽ��A��_____________ B��_____________ E��_____________ F��______________
(2)���2mol Na2O2������ˮ������Ӧ���ɵñ�״������������_________L��ͬʱ��Ӧ��ת�Ƶ���������____________��(NA��ʾ�����ӵ�����)
(3)���A��B�������3.0g(ƽ��Ħ������15g��mol��1)������G��ַ�Ӧ��ͨ������Na2O2�㣬��ʹNa2O2����__________g�����õ�O2_________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ǽ��������У���������Ҫ��ɫ�����������֪ʶ�ش��������⣺
(1)���зdz���Ҫ����;����д�����е�һ�֣�_________________________________��
(2)�Ŵ����������ϳɷ�һֱ�Ǹ��գ���������ѧ�Ҳŵ�֪���Ϊ�����Σ�������ɫ�Ĺ���ͭ��(BaCuSi2Ox��ͭΪ��2��)�����й��ڹ���ͭ����˵������ȷ����________��
A��������������ʽ��ʾΪBaO��CuO��2SiO2
B�������ȶ���������ɫ
C��x����6
D�����ܽ���ǿ���ǿ��
(3)��ҵ���ᴿ���ж���·�ߣ�����һ�ֹ�������ʾ��ͼ���£�

���ڵ绡¯�з����ķ�Ӧ��Ҫ�ڸ����������У�д���÷�Ӧ��ѧ����ʽ��________________��
��SiCl4����ˮ�⣬�ڿ����������̳��Ͱ������Ʋ���д��ˮ��Ļ�ѧ����ʽΪ____________________��
������������Ӧ�IJ����У���SiCl4�⣬����SiHCl3��SiH2Cl2��SiH3Cl��FeCl3�ȣ��й����ʵķе��������±�������SiCl4���������ʵķ���Ϊ________��
���� | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
�е�/�� | 2355 | 57.6 | 31.8 | 8.2 | ��30.4 | ��84.9 | ��111.9 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com