
”¾ĢāÄæ”æijӊ»śĪļÓÉC”¢H”¢OČżÖÖŌŖĖŲ×é³É£¬·Ö×ÓÖŠŗ¬ÓŠ8øöŌ×Ó£¬1moløĆÓŠ»śĪļŗ¬ÓŠ46molÖŹ×Ó£®ĶźČ«Č¼ÉÕøĆÓŠ»śĪļŌŚĻąĶ¬Ģõ¼žĻĀ²ā¶ØCO2ŗĶĖ®ÕōĘųĢå»ż±ČĪŖ2£ŗ1£®Č”2.7gøĆÓŠ»śĪļĒ”ŗĆÓė30mL 1mol/LµÄĢ¼ĖįÄĘČÜŅŗĶźČ«·“Ó¦£®£ØĒėŠ“³ö±ŲŅŖµÄ¼ĘĖć¹ż³Ģ£©Ēó£ŗ
£Ø1£©ÓŠ»śĪļ·Ö×ÓŹ½£»
£Ø2£©ÓŠ»śĪļ½į¹¹¼ņŹ½£®
£Ø3£©Š“³öøĆÓŠ»śĪļŌŚŅ»¶ØĢõ¼žĻĀÓėŅŅ¶ž“¼·“Ӧɜ³ÉĮłŌŖ»·×“»ÆŗĻĪļµÄ·½³ĢŹ½£®
”¾“š°ø”æ
£Ø1£©½ā£ŗøł¾ŻCO2ŗĶĖ®ÕōĘųĢå»ż±ČĪŖ2£ŗ1µĆ£¬N£ØC£©£ŗN£ØH£©=1£ŗ1£¬
”ąÉčøĆÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖCxHxOy£Øx”Ż1£¬y”Ż1£¬2x+y=8£©£¬
Čōx=1£¬y=6£¬ÖŹ×Ó×ÜŹż³¬¹ż46£¬²»·ūŗĻĢāŅā£¬
Čōx=2£¬y=4£¬ÖŹ×Ó×ÜŹż=6”Į2+1”Į2+8”Į4=46£¬·ūŗĻĢāŅā£®
”ąÉčøĆÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖC2H2O4£¬
“š£ŗÓŠ»śĪļ·Ö×ÓŹ½ĪŖC2H2O4£»
£Ø2£©½ā£ŗøĆÓŠ»śĪļµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ90£¬
2.7gøĆÓŠ»śĪļµÄĪļÖŹµÄĮæĪŖ0.03mol£¬Ģ¼ĖįÄʵÄĪļÖŹµÄĮæĪŖ0.03mol£¬
”ąøĆÓŠ»śĪļŗ¬Į½øöōČ»ł£¬½į¹¹¼ņŹ½HOOC©COOH£¬
“š£ŗÓŠ»śĪļµÄ½į¹¹¼ņŹ½ĪŖ£ŗHOOC©COOH£»
£Ø3£©½ā£ŗøĆÓŠ»śĪļŌŚŅ»¶ØĢõ¼žĻĀÓėŅŅ¶ž“¼·“Ӧɜ³ÉĮłŌŖ»·×“»ÆŗĻĪļµÄ·½³ĢŹ½ĪŖHOOC©COOH+HOH2C©CH2OH ![]()
 +2H2O£¬
+2H2O£¬
”¾½āĪö”æŌŚĻąĶ¬Ģõ¼žĻĀ²āµĆ²śĪļCO2ĘųĢåŗĶĖ®ÕōĘųµÄĢå»ż±ČĪŖ2£ŗ1£¬ÓŠ»śĪļAÖŠĢ¼Ō×ÓÓėĒāŌ×ÓĪļÖŹµÄĮæ±ČĪŖ2£ŗ1”Į2=1£ŗ1£¬ 2.7gøĆÓŠ»śĪļĒ”ŗĆÓė30mL 1mol/LµÄĢ¼ĖįÄĘČÜŅŗĶźČ«·“Ó¦£¬ŌņøĆÓŠ»śĪļÖŠŗ¬ÓŠōČ»ł£¬øł¾Ż2©COOH”«Na2CO3¹ŲĻµŹ½æÉÖŖ£¬ōČ»łµÄĪļÖŹµÄĮæ¾ĶµČÓŚĢ¼ĖįĒāÄʵÄĪļÖŹµÄĮæµÄ2±¶£¬Č»ŗóĢÖĀŪ³öAµÄĦ¶ūÖŹĮ棬ŌŁŠ“³É·Ö×ÓŹ½ŗĶ½į¹¹¼ņŹ½£¬ŅŌ“Ė½ā“šøĆĢā£®


 ³õÖŠŹīĘŚĻĪ½ÓĻµĮŠ“š°ø
³õÖŠŹīĘŚĻĪ½ÓĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖA”¢B”¢C”¢DŹĒ֊ѧ»Æѧ³£¼ūĪļÖŹ£¬ĖüĆĒŌŚŅ»¶ØĢõ¼žĻĀÓŠA+B”śC+DµÄ×Ŗ»Æ¹ŲĻµ”£
£Ø1£©ČōAĪŖ½šŹōĀĮ£¬BĪŖŃõ»ÆĢś£¬øĆ·“Ó¦µÄŅ»ÖÖÓĆĶ¾ŹĒ_______________”£
£Ø2£©ČōAŹĒŅ»ÖÖÄÜŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±äĄ¶µÄĘųĢ壬ĒŅøĆ·“Ó¦ŹĒ¹¤ŅµÉĻÖĘČ”ĻõĖįµÄÖŲŅŖ·“Ó¦Ö®Ņ»£¬øĆ·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ____________________________”£
£Ø3£©ČōAŹĒµ»ĘÉ«·ŪÄ©£¬³£ÓĆ×÷¹©Ńõ¼Į£¬CĪŖĒæ¼ī£¬ŌņøĆ·“Ó¦µÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ__________”£
£Ø4£©ČōAŹĒŅ»ÖÖĖįŹ½ŃĪ£¬æÉ×÷ĪŖŹ³Ę·ÖĘ×÷¹ż³ĢÖŠµÄÅņĖɼĮ£¬A”¢B”¢DČÜÓŚĖ®Ź±¾ł³Ź¼īŠŌ£¬ŌņøĆ·“Ó¦µÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“Ó»·¼ŗĶéæÉÖʱø1£¬4©»·¼ŗ¶ž“¼¶ž“×Ėįõ„£¬ĻĀĮŠ¹ż³ĢŹĒÓŠ¹ŲµÄ8²½·“Ó¦£ØĘäÖŠĖłÓŠĪŽ»ś²śĪļ¶¼ŅŃĀŌČ„£©£ŗ 
£Ø1£©ÉĻŹö¢Ł”«¢ą8øö²½ÖčÖŠŹōÓŚČ”“ś·“Ó¦µÄŹĒ£ØĢīŠņŗÅ£¬ĻĀĶ¬£©£»ŹōÓŚĻūČ„·“Ó¦µÄŹĒ£»ŹōÓŚ¼Ó³É·“Ó¦µÄŹĒ £®
£Ø2£©Š“³öĻĀĮŠĪļÖŹµÄ½į¹¹¼ņŹ½£ŗ
B £¬ C £¬ D £®
£Ø3£©Š“³öĻĀĮŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
¢Ś £»
¢Ż £»
¢Ž £®
¢ß £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄų¼°Ęä»ÆŗĻĪļŌŚ¹¤ŅµÉś²śŗĶæĘŃŠĮģÓņÓŠÖŲŅŖµÄÓĆĶ¾”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©»łĢ¬ Ni Ō×ÓÖŠ£¬µē×ÓĢī³äµÄÄÜĮæ×īøßµÄÄܼ¶·ūŗÅĪŖ_________£¬¼Ū²ćµē×ӵĹģµĄ±ķ“ļŹ½ĪŖ_________”£
£Ø2£©NiµÄĮ½ÖÖÅäŗĻĪļ½į¹¹ČēĶ¼ĖłŹ¾£ŗ
A B
¢ŁA µÄČŪ”¢·ŠµćøßÓŚBµÄŌŅņĪŖ_________”£
¢ŚA¾§Ģåŗ¬ÓŠ»Æѧ¼üµÄĄąŠĶĪŖ___________£ØĢīŃ”Ļī×ÖÄø£©”£
A£®¦Ņ¼ü B£®¦Š¼ü C£®ÅäĪ»¼ü D£®½šŹō¼ü
¢ŪA¾§ĢåÖŠNŌ×ÓµÄŌӻƊĪŹ½ŹĒ_________”£
£Ø3£© ČĖ¹¤ŗĻ³ÉµÄÉé»ÆÄų³£“ęŌŚø÷ÖÖȱĻŻ£¬Ä³Č±ĻŻÉé»ÆÄųµÄ×é³ÉĪŖNi1.2As£¬ ĘäÖŠ Ni ŌŖĖŲÖ»ÓŠ£«2 ŗĶ£«3 Į½ÖÖ¼ŪĢ¬£¬ Į½ÖÖ¼ŪĢ¬µÄÄųĄė×ÓŹżÄæÖ®±ČĪŖ_________”£
£Ø4£© NiAsµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£ŗ

¢ŁÄųĄė×ÓµÄÅäĪ»ŹżĪŖ_________”£
¢ŚČō°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµĪŖNA£¬¾§ĢåĆܶČĪŖ ¦Ń g”¤cm£3£¬ŌņøĆ¾§°ūÖŠ×ī½üµÄÉéĄė×ÓÖ®¼äµÄ¾ąĄėĪŖ_________pm”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æMg©AgClµē³ŲŹĒŅ»ÖÖŅŌŗ£Ė®ĪŖµē½āÖŹČÜŅŗµÄĖ®¼¤»īµē³Ų£®ĻĀĮŠŠšŹö“ķĪóµÄŹĒ£Ø””””£©
A.øŗ¼«·“Ó¦Ź½ĪŖMg©2e©=Mg2+
B.Õż¼«·“Ó¦Ź½ĪŖAg++e©=Ag
C.µē³Ų·ÅµēŹ±Cl©ÓÉÕż¼«Ļņøŗ¼«ĒØŅĘ
D.øŗ¼«»į·¢Éśø±·“Ó¦Mg+2H2O=Mg£ØOH£©2+H2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĻĀĮŠŹµŃéŹĀŹµ£ŗ
£Ø1£©X£«Y2£«===X2£«£«Y
£Ø2£©Z£«2H2O![]() Z(OH)2£«H2”ü
Z(OH)2£«H2”ü
£Ø3£©Z2£«Ąė×ÓµÄŃõ»ÆŠŌ±ČX2£«Čõ
£Ø4£©ÓÉY”¢W×÷µē¼«×é³ÉµÄŌµē³Ų·“Ó¦ĪŖ£ŗY£2e£===Y2£«
ÓÉ“ĖæÉÖŖ£¬X”¢Y”¢Z”¢WµÄ»¹ŌŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ£Ø£©
A. X£¾Y£¾Z£¾W B. Y£¾X£¾W£¾Z
C. Z£¾X£¾Y£¾W D. Z£¾Y£¾X£¾W
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ0.25 mol Na2SO4ÖŠ£¬ŗ¬ÓŠµÄŃõŌ×ÓøöŹżŌ¼ĪŖ
A.1B.0.25
C.6.02”Į1023D.3.01”Į1023
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆ·“Ó¦6NO2£«8NH3===7N2£«12H2O¹¹³Éµē³ŲµÄ×°ÖĆČēĶ¼ĖłŹ¾”£“Ė·½·Ø¼ČÄÜŹµĻÖÓŠŠ§Ēå³żµŖŃõ»ÆĪļµÄÅÅ·Å£¬¼õĒį»·¾³ĪŪČ¾£¬ÓÖÄܳä·ÖĄūÓĆ»ÆѧÄÜ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©

A. µēĮ÷“Ó×ó²ąµē¼«¾¹żøŗŌŲŗóĮ÷ĻņÓŅ²ąµē¼«
B. ĪŖŹ¹µē³Ų³ÖŠų·Åµē£¬Ąė×Ó½»»»Ä¤ŠčŃ”ÓĆŅõĄė×Ó½»»»Ä¤
C. µē¼«A¼«·“Ó¦Ź½ĪŖ2NH3£6e£===N2£«6H£«
D. µ±ÓŠ4.48 L NO2±»“¦ĄķŹ±£¬×ŖŅʵē×ÓŹżĪŖ0.8NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŗćĪĀĢõ¼žĻĀĘšŹ¼Ź±ČŻ»ż¾łĪŖ5LµÄ¼×”¢ŅŅĮ½ĆܱÕČŻĘ÷ÖŠ£Ø¼×ĪŖŗćČŻČŻĘ÷”¢ŅŅĪŖŗćŃ¹ČŻĘ÷£©£¬¾ł½ųŠŠ·“Ó¦£ŗN2£Øg£©+3H2£Øg£©2NH3£Øg£©”÷H2=©92.4kJ/mol£¬ÓŠ¹ŲŹż¾Ż¼°ĢŲ¶ØĘ½ŗāדĢ¬¼ū±ķ£®
ČŻĘ÷ | ĘšŹ¼Ķ¶Čė | “ļĘ½ŗāŹ± | |||
¼× | 2molN2 | 3molH2 | 0molNH3 | 1.5molNH3 | |
ŅŅ | amolN2 | bmolH2 | 0molNH3] | 1.2molNH3 | |
£Ø1£©ČōĘ½ŗāŗóĶ¬ÖÖĪļÖŹµÄĢå»ż·ÖŹżĻąĶ¬£¬ĘšŹ¼Ź±ŅŅČŻĘ÷ĶØČėµÄN2µÄĪļÖŹµÄĮæĪŖ £¬
ĘšŹ¼Ź±ŅŅÖŠµÄŃ¹ĒæŹĒ¼×ČŻĘ÷µÄ±¶£¬ŅŅµÄĘ½ŗā³£ŹżĪŖ
£Ø2£©ŗćČŻĆܱÕČŻĘ÷ÖŠæÉŅŌ·¢Éś°±ĘųµÄ·Ö½ā·“Ó¦£¬“ļĘ½ŗāŗ󣬽öøıäĻĀ±ķÖŠ·“Ó¦Ģõ¼žx£¬ĻĀĮŠø÷ĻīÖŠyĖęxµÄŌö“ó¶ųŌö“óµÄŹĒ£ØŃ”ĢīŠņŗÅ£©£®
Ń”Ļī | a | b | c | d |
x | ĪĀ¶Č | ĪĀ¶Č | ¼ÓČėH2µÄĪļÖŹµÄĮæ | ¼ÓČė°±ĘųµÄĪļÖŹµÄĮæ |
y | »ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ | Ę½ŗā³£ŹżK | »ģŗĻĘųĢåµÄĆÜ¶Č | “ļĘ½ŗāŹ±°±ĘųµÄ×Ŗ»ÆĀŹ |
£Ø3£©ŃŠ¾æŌŚĘäĖūĢõ¼ž²»±äŹ±£¬øıäĘšŹ¼ĪļĒāĘųµÄĪļÖŹµÄĮæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ŹµŃé½į¹ūČēĶ¼ĖłŹ¾£ØĶ¼ÖŠT±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩£ŗ
¢ŁĻńÖŠT2ŗĶT1µÄ¹ŲĻµŹĒ£ŗT2T1£ØĢī”°øßÓŚ”±”°µĶÓŚ”±”°µČÓŚ”±”°ĪŽ·ØČ·¶Ø”±£©£®
¢Śa”¢b”¢cČżµćÖŠ£¬N2×Ŗ»ÆĀŹ×īøߵďĒ£ØĢī×ÖÄø£©£®
¢ŪČōČŻĘ÷ČŻ»żĪŖ1L£¬T2”ęŌŚĘšŹ¼ĢåĻµÖŠ¼ÓČė1mol N2 £¬ 3molH2 £¬ ¾¹ż5min·“Ó¦“ļµ½Ę½ŗāŹ±H2µÄ×Ŗ»ÆĀŹĪŖ60%£¬ŌņNH3µÄ·“Ó¦ĖŁĀŹĪŖ £® ±£³ÖČŻĘ÷Ģå»ż²»±ä£¬ČōĘšŹ¼Ź±ĻņČŻĘ÷ÄŚ·ÅČė2mol N2ŗĶ6mol H2 £¬ “ļĘ½ŗāŗó·Å³öµÄČČĮæĪŖQ£¬ŌņQ110.88kJ£ØĢī”°£¾”±”¢”°£¼”±»ņ”°=”±£©£®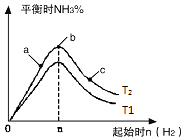
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com