
(7分)实验室利用如图装置进行中和热的测定,请回答下列问题:
(1)在操作正确的前提下,提高中和热测定准确性的关键是
(2)做1次完整的中和热测定实验,温度计需使用 次,某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?
(3)请为本实验设计数据记录表格:
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
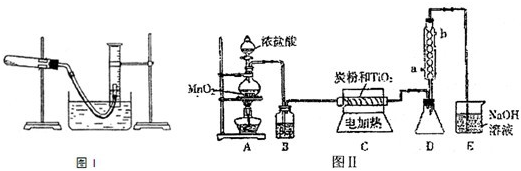
| 编号 | 装置的缺陷和不妥之处 |
| a | TiCl4 遇空气中水蒸气发生水解,缺少阻止水蒸气进入D的装置 TiCl4 遇空气中水蒸气发生水解,缺少阻止水蒸气进入D的装置 |
| b | TiCl4 水解产生的氯化氢极易溶于水,需要加上防倒吸的装置 TiCl4 水解产生的氯化氢极易溶于水,需要加上防倒吸的装置 |
| … | 由于CO气体有毒,缺少CO的处理装置 由于CO气体有毒,缺少CO的处理装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
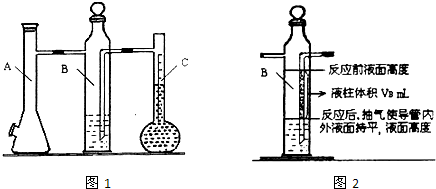
| 实验次数 | m(Mg)/g | 硫酸体积/mL | 液体量瓶中液体体积/mL | 抽出气体体积/mL | 氢气体积/mL | 计算1mol氢体积/L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | X | |
| 2 | 0.115 | 10.0 | 121.0 | 8.0 |
| 实验次数 | m(Mg) g |
硫酸体积mL | 液体量瓶中液体体积mL | 抽出气体体积mL | B瓶的一段液柱体积mL | 水汽体积百分含量 | 计算1mol氢体积L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | VB | a% |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年吉林省九校联合体高三第二次摸底考试理综化学试卷(解析版) 题型:实验题
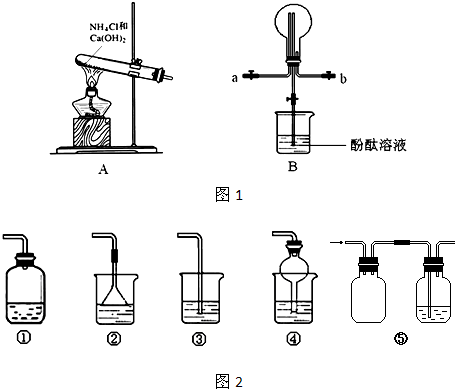
某兴趣小组在实验室用加热乙醇、浓H2SO4、溴化钠和少量水的混合物来制备溴乙烷,检验反应的部分副产物,并探究溴乙烷的性质。
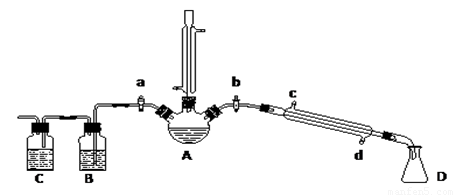
(一)溴乙烷的制备及产物的检验:设计了如上图装置,其中夹持仪器、加热仪器及冷却水管没有画出。请根据实验步骤,回答下列问题:
(1)竖直冷凝管冷凝水流向 口进 口出,竖直冷凝管冷凝的作用
(2)制备操作中,加入的少量的水,其目的是 ;(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(3)该实验装置中 装置可防止倒吸,中学化学实验中 用此方法防止倒吸。
(4)理论上,上述反应的副产物还可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、溴化氢等:检验副产物中是否含有溴化氢:熄灭酒精灯,在竖直冷凝管上方塞上塞子、打开a,利用余热继续反应直至冷却,通过B、C装置检验。B、C中应盛放的试剂分别是 、 。
(5)欲除去溴乙烷中的少量杂质Br2,下列物质中最适合的是 。(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl
(二)溴乙烷性质的探究:
用如图实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:

Ⅰ:在试管中加入10 mL6mol/L NaOH溶液和2 mL 溴乙烷,振荡。
II:将试管如图固定后,水浴加热。
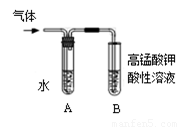
(6)观察到___________现象时,表明溴乙烷与NaOH溶液已完全反应。
(7)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,将生成的气体通入 如图装置。A试管中的水的作用是 ,若无A试管,B试管中的试剂应为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com