
| A. | 稳定性:H2O<H2S<H2Se | |
| B. | 降温有利于Se与H2反应生成H2Se | |
| C. | O2(g)+2H2S(g)═2H2O(g)+2S(g)△H=-444 kJ•mol-1 | |
| D. | 随着核电荷数的增加,VIA族元素单质与H2的化合反应越容易发生 |
分析 A.相同物质的量的O2、S、Se三种物质,与氢气反应,生成物的能量越高,稳定性越差;
B.Se与H2反应为吸热反应,升高温度有利于反应进行;
C.根据已知方程式构建目标方程式,结合盖斯定律进行解答;
D.生成物的氢化物越稳定,其元素单质与H2的化合反应越容易.
解答 解:A.$\frac{1}{2}$O2(g)+H2(g)═H2O(g)△H=-242kJ•mol-1,O2(g)+2H2(g)═2H2O(g)△H=-484kJ•mol-1,相同物质的量的O2、S、Se三种物质,与氢气反应,O2释放的能量最多,Se需吸收能量,能量越高,稳定性越差,所以稳定性:H2O>H2S>H2Se,故A错误;
B.Se(g)+H2(g)?H2Se(g)△H=+81kJ•mol-1,该反应为吸热反应,升高温度有利于Se与H2反应生成H2Se,故B错误;
C.已知:①$\frac{1}{2}$O2(g)+H2(g)═H2O(g)△H=-242kJ•mol-1②S(g)+H2(g)═H2S(g)△H=-20kJ•mol-1,将①×2-②得O2(g)+2H2S(g)═2H2O(g)+2S(g)△H=-444 kJ•mol-1,故C正确;
D.由A选项分析可知稳定性:H2O>H2S>H2Se,生成物的氢化物越稳定,其元素单质与H2的化合反应越容易,所以随着核电荷数的增加,VIA族元素单质与H2的化合反应越难发生,故D错误;
故选C.
点评 本题考查了反应热的计算、元素周期律的应用,掌握盖斯定律的应用以及非金属性的递变规律是解答关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 原子半径(nm) | 0.075 | 0.110 | 0.152 | 0.071 | 0.186 | 0.099 |
| 最高价态 | +5 | +5 | +1 | 0 | +1 | +7 |
| 最低价态 | -3 | -3 | 0 | -1 | 0 | -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
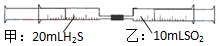 常温下,将甲针筒内20mLH2S推入含有10mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )
常温下,将甲针筒内20mLH2S推入含有10mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )| A. | 有淡黄色固体生成 | B. | 有无色液体生成 | ||
| C. | 气体体积缩小 | D. | 最终约余15mL气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 溶解度(s)/g | 溶度积(Ksp) | 摩尔质量(M)g/mol | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
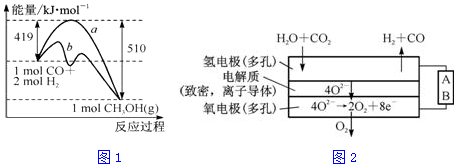
| 化学键 | C-C | C-H | H-H | C-O | C≡O | O-H |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | x | 463 |
| 离子 | Cu2+ | H+ | Cl- | SO42 - |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
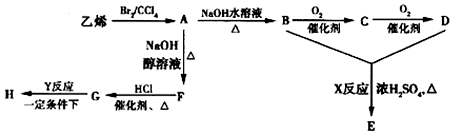
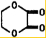 +2H2O;
+2H2O; +2NaOH$\stackrel{△}{→}$NaOOCCOONa+HOCH2CH2OH.
+2NaOH$\stackrel{△}{→}$NaOOCCOONa+HOCH2CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
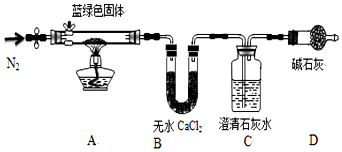
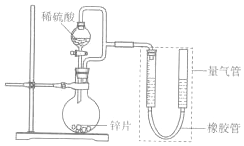 某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:
某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:| 序号 | V(H2SO4)/mL | C(H2SO4)/mol•L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它是一种共价化合物 | |
| B. | 它只含共价键 | |
| C. | 它不可能与NaOH溶液反应 | |
| D. | 它受热时,可能会分解产生有色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com