
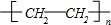 ;
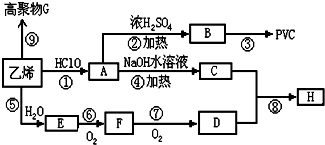
;分析 乙烯发生加聚反应得到高聚物G为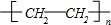 ,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为
,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为 ,据此解答.
,据此解答.
解答 解:(1)由上述分析可知,B的结构简式为CH2=CHCl,G的结构简式为: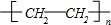 ,故答案为:CH2=CHCl;
,故答案为:CH2=CHCl;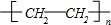 ;
;
(2)D(CH3COOH)的同分异构体的结构简式为:HCOOCH3、HOCH2CHO,故答案为:HCOOCH3或HOCH2CHO;
(3)A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,化学方程式为:HOCH2CH2Cl+NaOH→HOCH2CH2OH+NaCl+H2O,
故答案为:HOCH2CH2Cl+NaOH→HOCH2CH2OH+NaCl+H2O;
(4)反应⑥是乙醇氧化生成乙醛,反应化学方程式为:2C2H5OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,故答案为:2C2H5OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;氧化反应.
点评 本题考查有机物推断,涉及烯、醇、醛、羧酸之间的转化关,难度不大,注意基础知识的理解掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池中电解质溶液能电离出自由移动的离子 | |
| B. | 有两根导线将两个活动性不同的电极连接 | |
| C. | 电极上进行的氧化还原反应的生成物为电子 | |
| D. | 电极上进行氧化还原反应时有电子的定向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应是吸热反应,且A是气态 | |
| B. | 正反应是放热反应,且A不是气态 | |
| C. | 其他条件不变,加入少量A,该平衡不移动 | |
| D. | 改变压强对该平衡的移动无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用分液漏斗分离溴和四氯化碳 | |
| B. | CH3COOCH3核磁共振氢谱中只给出一种信号 | |
| C. | 乙醇(CH3CH2OH)和二甲醚(CH3-O-CH3)互为碳链异构体 | |
| D. | 与氢气加成得到2,3-二甲基戊烷的烯烃结构式有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律 | |
| B. | IA族与ⅦA族元素间可形成离子键也可形成共价键 | |
| C. | Cl-、S2-、Ca2+、K+半径逐渐减小 | |
| D. | 同周期金属元素的化合价越高,其原子失电子能力越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO、NO能与人体的血红蛋白结合,使人中毒 | |
| B. | CaO能与SO2反应,可作工业废气的脱硫剂 | |
| C. | 光化学烟雾会引起呼吸道疾病 | |
| D. | CO2、NO2或SO2都会导致酸雨的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | B. | 乙烯的分子式:C2H4 | ||
| C. | 乙酸的结构简式:C2H4O2 | D. | 丙烷分子的球棍模型是 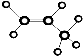 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 电极甲 | 电极乙 |
| I | Zn | Cu |
| Ⅱ | Al | Cu |
| A. | 两组实验溶液的pH均增大 | |
| B. | 实验Ⅱ中,H+向Al定向迁移 | |
| C. | 实验I中,甲电极反应为:2H++e-=H2↑ | |
| D. | 实验Ⅱ中,电子由铜转移到锌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com