
| A. | CCl4可用于鉴别溴水和碘水 | |
| B. | 甲苯(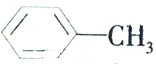 )中所有原子都在同一平面内 )中所有原子都在同一平面内 | |
| C. | 1mol甲苯含有6NA个C-H键 | |
| D. | 苯与甲苯互为同系物,均能使酸性KMnO4溶液褪色 |
分析 A.四氯化碳萃取溶液中的溴、碘,分别呈橙红色、紫红色;
B.含有甲基,具有四面体结构;
C.甲苯分子中含有8个C-H键;
D.苯不能使酸性高锰酸钾溶液褪色.
解答 解:A.四氯化碳萃取溶液中的溴、碘,分别呈橙红色、紫红色,现象不同,可以区别,故A正确;
B.含有甲基,具有四面体结构,所有原子不可能都在同一平面内,当碳原子都处于同一平面内,故B错误;
C.甲苯分子中含有8个C-H键,1mol甲苯含有8NA个C-H键,故C错误;
D.苯与甲苯属于同系物,甲苯可以使酸性高锰酸钾溶液褪色,但苯不能,故D错误,
故选:A.
点评 本题考查有机物的结构与性质、有机物的鉴别,难度不大,注意苯的同系物中连接苯环的碳原子上含有H原子的可以被酸性高锰酸钾溶液氧化.


科目:高中化学 来源: 题型:选择题
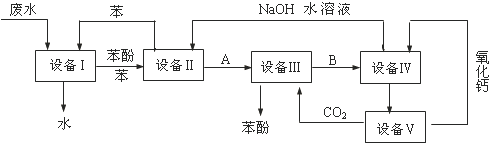
| A. | 上述流程里,设备Ⅰ、Ⅱ中进行的是分液操作;实验室里该操作可以用分液漏斗进行 | |
| B. | 上述流程里,设备Ⅲ、Ⅳ中进行的是过滤操作;实验室里该操作用到的玻璃仪器有:漏斗、烧杯、玻璃棒 | |
| C. | 在设备Ⅲ中发生反应的化学方程式为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 | |
| D. | 图中循环使用的物质是C6H6、CaO、CO2和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
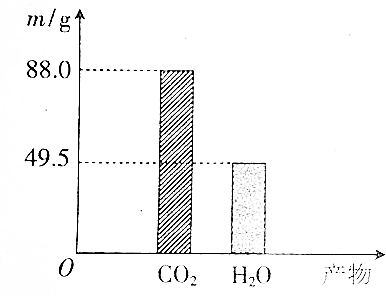
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂 | B. | 油漆 | C. | 石油 | D. | 煤焦油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.5mol单质Fe粉在足量氧气中完全燃烧,失去4NA个电子 | |
| B. | 在25g质量分数为60%的乙酸水溶液中,含有氢原子数为NA | |
| C. | 7.8 gNa2S和Na2O2 的混合物中,含有的阴离子数等于0.15NA | |
| D. | 在5×107Pa、500°C和铁触媒作用下,1molN2和3molH2可生成氨气分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
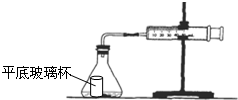 盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:
盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 |
| 气体体积/mL | 4 | 14 | 25 | 38 | 47 | 55 |
| 反应速率/mL•s-1 | 0.4 | 1.0 | 1.1 | 1.3 | 0.9 | 0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
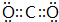 .D2A2中所含化学键类型为非极性共价键和离子键.
.D2A2中所含化学键类型为非极性共价键和离子键. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com