
| A、C3H8 |
| B、C3H6 |
| C、C4H8 |
| D、C4H6 |
| m |
| M |
| 11g |
| 44g/mol |
| 16.8L |
| 22.4L/mol |
| 2g |
| 1g/mol |
| 0.75mol |
| 0.25mol |
| 2mol |
| 0.25mol |


科目:高中化学 来源: 题型:
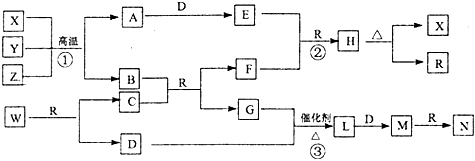
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向煮沸的1mol/L NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体 |
| B、光线透过胶体时,胶体发生丁达尔效应 |
| C、直径介于1nm--100nm之间的微粒称为胶体 |
| D、分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
| B、氯气通入氢氧化钠溶液中:2Cl2+2OH-═3Cl-+ClO-+H2O |
| C、氯化亚铁溶液中滴加过量新制氯水:2Fe2++Cl2═2Fe3++2Cl- |
| D、少量碳酸钙固体加入足量稀盐酸中:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液加到醋酸溶液中:Ca(HCO3)2+2CH3COOH═Ca2++2CH3COO-+2CO2↑+2H2O | ||||
B、用惰性电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| C、电解精炼铜的阳极反应式只有:Cu-2e-=Cu2+ | ||||
| D、在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:Y>Z>X |
| B、Y的气态氢化物的热稳定性比R的强 |
| C、R的最高价氧化物的水化物酸性比W的强 |
| D、Y与Z形成的化合物只有1种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该合金中镁与铜的物质的量之比是1:2 |
| B、NO2和N2O4的混合气体中,N2O4的体积分数是80% |
| C、得到5.08g沉淀时,加入NaOH溶液的体积是620mL |
| D、该反应中共转移电子为1.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com