
【题目】水杨酸某酯E的合成路线如图所示: 
已知:①2RCH2CHO ![]() R﹣
R﹣ ![]()
②A分子中只含有1个甲基;③D的相对分子质量为130;
(1)C中含氧官能团的名称为;反应④的反应方程式为;
(2)在合成路线中,设计⑤和⑦的目的;
(3)X是B的最简单同系物,请写出X与足量银氨溶液反应的离子方程式;
(4)下列有关说法正确的是;
a.B中有4种不同的氢
b.水杨酸与足量NaHCO3反应生成 ![]()
c.D不与金属钠反应
d.1mol E与氢气加成,最多消耗4mol H2
(5)H有多种同分异构体,其中能同时满足下列条件的共有种(不考虑立体异构)
①能发生银镜反应;②能发生水解反应;③能与FeCl3溶液发生显色反应,其中有5种氢,且氢的个数比为1:1:2:2:2的为(写结构简式).
【答案】
(1)醛基;CH3CH2CH2CH2CH(CH2CH3)CH2OH+ 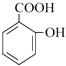 →
→ 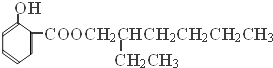 +H2O
+H2O
(2)防止苯环上的酚羟其被氧化
(3)HCHO+4[Ag(NH3)2]++4OH﹣ ![]() ?CO32++2NH4++4Ag↓+6NH3+2H2O
?CO32++2NH4++4Ag↓+6NH3+2H2O
(4)a
(5)13;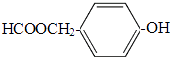
【解析】解:A的分子式为C4H10O,分子中只含有1个甲基,可以发生催化氧化,则A的结构简式为CH3CH2CH2CH2OH,B的结构简式为CH3CH2CH2CHO,由题目信息可知C的结构简式为CH3CH2CH2CH=C(CH2CH3)CHO,D的相对分子质量为130,比C的相对分子质量大4,E为水杨酸酯,则D结构简式为CH3CH2CH2CH2CH(CH2CH3)CH2OH,C和氢气发生加成反应生成D,D和邻羟基苯甲酸发生酯化反应生成E,E结构简式为 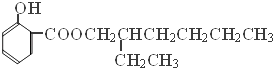 ,F发生取代反应生成G,G发生氧化反应生成H,H发生取代反应生成水杨酸,设计⑤和⑦的目的防止苯环上的酚羟其被氧化.
,F发生取代反应生成G,G发生氧化反应生成H,H发生取代反应生成水杨酸,设计⑤和⑦的目的防止苯环上的酚羟其被氧化.
(1.)C的结构简式为CH3CH2CH2CH=C(CH2CH3)CHO,C中含氧官能团的名称为醛基,反应④的反应方程式为:CH3CH2CH2CH2CH(CH2CH3)CH2OH+ 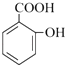 →
→ 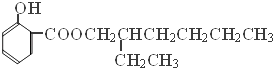 +H2O,
+H2O,
所以答案是:醛基;CH3CH2CH2CH2CH(CH2CH3)CH2OH+ 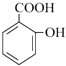 →
→  +H2O;
+H2O;
(2.)在合成路线中,设计⑤和⑦的目的:防止苯环上的酚羟其被氧化,所以答案是:防止苯环上的酚羟其被氧化;
(3.)X是B的最简单同系物,则X为HCHO,与足量银氨溶液反应的离子方程式:HCHO+4[Ag(NH3)2]++4OH﹣ ![]() CO32++2NH4++4Ag↓+6NH3+2H2O,所以答案是:HCHO+4[Ag(NH3)2]++4OH﹣
CO32++2NH4++4Ag↓+6NH3+2H2O,所以答案是:HCHO+4[Ag(NH3)2]++4OH﹣ ![]() CO32++2NH4++4Ag↓+6NH3+2H2O;
CO32++2NH4++4Ag↓+6NH3+2H2O;
(4.)a.B为CH3CH2CH2CHO,有4种不同的氢,故a正确;
b.羧基能与碳酸氢钠反应,而酚羟基不能够与碳酸氢钠反应,故b错误;
c.D中含有醇羟基,能与金属钠反应,故c错误;
d.E中苯环能与氢气发生加成反应,1mol E与氢气加成,最多消耗3mol H2 , 故d错误.
故选:a;
(5.)H有多种同分异构体,其中能同时满足下列条件:①能发生银镜反应,说明含有醛基②能发生水解反应,说明含有酯基,为甲酸形成的酯基,③能与FeCl3溶液发生显色反应,说明含有酚羟基,含有2个侧链,除酚羟基外,另外的取代基为﹣CH2OOCH,有邻、间、对3种,含有3个取代基为﹣OH、﹣CH3、﹣OOCH,当﹣OH、﹣CH3有邻、间、对3种位置,对应的﹣OOCH分别有4种、4种、2种位置,故符合条件的同分异构体共有13种,其中有5种氢,且氢的个数比为1:1:2:2:2的为 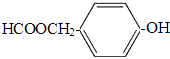 ,所以答案是:13;
,所以答案是:13; 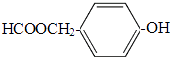 .
.


科目:高中化学 来源: 题型:
【题目】固体粉末X中可能含有K2SO3、K2CO3、FeO、Fe2O3、MnO2、Na2SO4、NaNO3中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下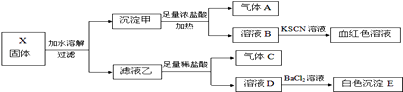
根据上述实验,下列说法正确的是 ( )
A.固体X中一定含有Fe2O3
B.沉淀E可能含有BaSO3
C.气体A,C一定均为纯净物
D.固体X可能出现含有K2SO3、K2CO3而不含Na2SO4的情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验氯化氢气体中是否混有Cl2,不能采用的方法是( )
A.用湿润的蓝色石蕊试纸B.用湿润的有色布条
C.将气体通入AgNO3溶液D.用湿润的淀粉碘化钾试纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( ) 
A.甲装置:可用来证明碳的非金属性比硅强
B.乙装置:橡皮管的作用是能使水顺利流下
C.丙装置:用图示的方法不能检查此装置的气密性
D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集一氧化氮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单晶硅是信息产业中重要的基础材料.通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硫、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450﹣500℃),四氯化硅经提纯后用氢气还原可得高纯硅.以下是实验室制备四氯化硅的装置示意图.
查阅相关资料获悉:
a.四氯化硅遇水极易水解;
b.铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
物质 | SiCl4 | AlCl3 | FeCl3 | PCl5 |
沸点/℃ | 57.7 | ﹣ | 315 | ﹣ |
熔点/℃ | ﹣70.0 | ﹣ | ﹣ | ﹣ |
升华温度/℃ | ﹣ | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式 .
(2)装置A中g管的作用是;装置C中的试剂是;装置E中的h瓶需要冷却理由是 .
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,含有铁、铝等元素的杂质.为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+ , 再用KMnO4标准溶液在酸性条件下进行氧化还原反应滴定,锰元素被还原为Mn2+ . ①写出用KMnO4滴定Fe2+的离子方程式:;
②滴定前是否要滴加指示剂?(填“是”或“否”),判断滴定终点的方法是 .
③某同学称取5.000g残留物,预处理后在容量瓶中配制成100ml溶液,移取25.00ml试样溶液,用1.000×10﹣2molL﹣1KMnO4标准溶液滴定.达到滴定终点时,消耗标准溶液20.00ml,则残留物中铁元素的质量分数是 . 若滴定前平视,滴定后俯视KMnO4液面,对测定结果有何影响(填“偏高”、“偏低”、或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量X和Y加入密闭容器,在一定条件下发生反应:X(g)+Y(g)Z (s)+2W(g),平衡时W的体积分数(%)随温度和压强的变化如表所示.
1.0 MPa | 2.0 MPa | 3.0 MPa | |
800℃ | a | b | 83% |
900℃ | c | 75% | d |
1000℃ | 54% | e | f |
①a>c>f ②900℃、2.0MPa时,X的转化率为75% ③该反应的△H<0 ④平衡常数K(1000℃)>K(800℃)上述①~④中正确的有( )
A.4个
B.3个
C.2个
D.1个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.3C(s)+CaC(s)?CaC2 (s)+CO(g)在常温下不能自发进行,说明该反应的△H>0
B.CH3COOH溶液加水稀释后,溶液中 ![]() 的值增大
的值增大
C.恒温恒压的密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g)△H=﹣aKJ/mol,平衡时向容器中在充入一定量的NH3 , 重新达到平衡时a值不变
D.C(s)+H2O(g)?CO(g)+H2(g) (△H>0),其它条件不变时,升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物{[Cr(CH3COO)2]22H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂,实验室中以锌粒,三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,且仪器2中预先加入锌粒,已知二价铬不稳定,极易被氧气氧化,不与锌反应.制备过程中发生的相关反应如下:
Zn(s)+2HCl(aq)═ZnCl2(aq)+H2(g)
2CrCl3(aq)+Zn(s)═2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO﹣(aq)+2H2O(l)═[Cr(CH3COO)2]22H2O(s)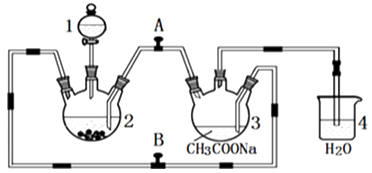
请回答下列问题:
(1)仪器1的名称是 .
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是(选下面的A、B或C);目的是 .
A.盐酸和三氯化铬溶液同时加入 B.先加三氯化铬溶液一段时间后再加盐酸C.先加盐酸一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭阀门(填“A”或“B”,下同),打开阀门 .
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应外,另一个作用是 .
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol/L;实验后得干燥纯净的[Cr(CH3COO)2]22H2O9.4g,则该实验所得产品的产率为(不考虑溶解的醋酸亚铬水合物).
(6)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+ , 最好往废液中通入足量的,再加入碱液,调节pH至少为才能使铬的离子沉淀完全(铬的离子浓度应小于10﹣5mol/L).【已知Cr(OH)3的溶度积为6.3×10﹣31 , ![]() ≈4,lg2≈0.3】
≈4,lg2≈0.3】
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com