
【题目】海洋是巨大的化学资源宝库,人类每年都会从海水中提取很多物质,如图是海水资源综合利用的部分流程。
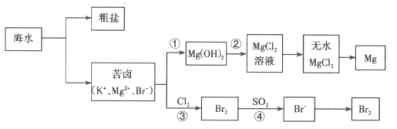
请回答下列问题:
(1)从海水中获取粗盐的方法是___。
(2)步骤①中所加试剂是___,步骤②中发生反应的离子方程式是___。
(3)步骤③中发生反应的离子方程式是___。
(4)步骤④中用“热空气”能从溶液中将Br2吹出的原因是___,用SO2水溶液吸收吹出的Br2时,反应过程中的氧化剂是___。
【答案】蒸发结晶 Ca(OH)2 Mg(OH)2+2H+=Mg2++2H2O Cl2+2Br-=2Cl-+Br2 Br2的挥发性随温度升高而增大 Br2
【解析】
将海水蒸发结晶可到粗盐,得到的苦卤含有钾离子,镁离子,溴离子,经步骤①加入氢氧化钙得到氢氧化镁,氢氧化镁经②加入盐酸得到氯化镁溶液,在充入氯化氢气体的溶液中加热蒸干得到无水氯化镁,电解熔融的氯化镁得到镁单质;步骤③为溴离子被氯气氧化成溴单质,步骤④将溴富集,用“热空气”能从溶液中将Br2吹出,再得到高纯度的溴,据此分析。
(1) 食盐的溶解度受温度影响变化不大,故要从海水中获得粗盐的结晶方法是蒸发结晶;
(2)根据分析可知,步骤①中所加试剂是氢氧化钙,将镁离子转化为氢氧化镁,步骤②是氢氧化镁和盐酸反应制得氯化镁的过程,发生反应的离子方程式是:Mg(OH)2+2H+=Mg2++2H2O;
(3)步骤③发生氯气与溴离子的反应,发生反应的离子方程式是:Cl2+2Br-=2Cl-+Br2;
(4)步骤④中用“热空气”能从溶液中将Br2吹出的原因是Br2的挥发性随温度升高而增大,用SO2水溶液吸收吹出的Br2时,溴和二氧化硫和水反应生成氢溴酸和硫酸,溴单质的化合价降低,故氧化剂是Br2。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】近期,柔性屏手机开始崭露头角。某柔性屏手机的柔性电池以碳纳米管做电极材料,以ZnSO4溶液的有机高聚物为固态电解质,其电池总反应为:MnO2+![]() Zn +(1+
Zn +(1+![]() )H2O+
)H2O+![]() ZnSO4
ZnSO4![]() MnOOH+
MnOOH+![]() ZnSO4·3Zn(OH)2·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。
ZnSO4·3Zn(OH)2·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。

下列说法中,正确的是
A.充电时,含有锌膜的碳纳米管纤维一端连接电源正极
B.放电时,电池的正极反应为:MnO2 + e- + H+ = MnOOH
C.充电时,Zn2+移向Zn膜
D.有机高聚物中的氢键是一种特殊的化学键,键能大于共价键,能使高聚物更稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用废干电池中黑色粉末(主要成分MnO2、炭粉及少量Hg2+、Pb2+等重金属盐)制备MnSO4晶体的工艺流程如图:
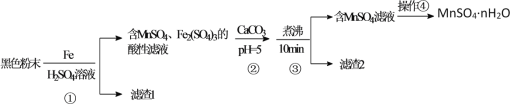
下列说法错误的是( )
A.反应①中1molFe至多还原1.5molMnO2
B.重金属主要在滤渣2中
C.步骤③煮沸可使沉淀颗粒长大,目的是便于固液分离
D.合理处理废旧电池有利于资源再利用并防止汞、铅等重金属污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH>4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.用0.2000mol/LNaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol/L),至中性时,溶液中的酸未被完全中和
D.室温下,将CH3COONa溶液加水稀释,溶液中![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等浓度的NaOH溶液分别滴加到等pH、等体积的HA、HB两种弱酸溶液中,溶液的pH与粒子浓度比值的对数关系如图所示。下列叙述错误的是( )
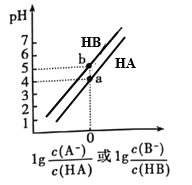
A. a点时,溶液中由水电离的c(OH-)约为1×10-10 mol·L-1
B. 电离平衡常数:Ka(HA)< Ka(HB)
C. b点时,c(B-)=c(HB)>c(Na+)>c(H+)>c(OH-)
D. 向HB溶液中滴加NaOH溶液至pH=7时:c(B-)> c(HB)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有C、H、O的化合物,其C、H、O的质量比为12∶1∶16,其蒸气相对于氢气的密度为58,它能与小苏打反应放出CO2,也能使溴水褪色,0.58g这种物质能与50mL0.2mol/L的氢氧化钠溶液完全反应。试回答:
(1)该有机物中各原子个数比N(C)∶N(H)∶N(O)= ______________
(2)该有机物的摩尔质量为__________,写出分子式_____________
(3)该有机物的可能结构简式有___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃条件下,用0.1molL-1的一元弱酸HR[已知:25℃时,Ka(HR)=1.7×10-5]溶液滴定10.00mL0.1molL-1一元碱MOH溶液,滴定过程中HR溶液的体积与溶液中lg![]() 的关系如图所示。下列说法正确的是( )
的关系如图所示。下列说法正确的是( )

A.25℃时,0.1molL-1的MOH溶液pH<13
B.a点消耗HR溶液的体积等于10.00mL
C.b点溶液中c(R-)>c(H+)>c(M+)>c(OH-)
D.25℃时,MR溶液中![]() =
=![]() ×10-9
×10-9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知电离常数的负对数pK=-lgK,25℃时,HX的pKa=4.76,H2Y的pKa1=1.22,pKa2=4.19,下列说法正确的是( )
A.浓度相等的NH4X和NH4HY溶液中c(NH4+):前者大于后者
B.NaX溶液中滴加KHY溶液至pH=4.76:c(K+)+c(Na+)>c(HY-)+2c(Y2-)+c(X-)
C.KHY溶液中滴加氨水至中性:c(NH4+)>c(Y2-)
D.K2Y溶液中滴加盐酸至pH=1.22:c(Cl-)-3c(HY-)=c(H+)-c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外实验小组利用压强传感器、数据采集器和计算机等数字化实验设备,探究用0.01g镁条分别与2mL不同浓度稀盐酸的反应速率。实验结果如图所示。
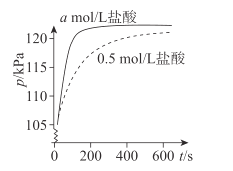
(1)Mg与盐酸反应的离子方程式是________。
(2)从微粒角度分析,该实验是为了探究________(因素)对该反应的化学反应速率的影响。
(3)a________0.5(填“>”或“<”)。
(4)如果用0.5mol/L硫酸代替上述实验中的0.5mol/L盐酸,二者的反应速率是否相同____,请说明原因:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com