
【题目】工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol, 则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0. 12 mol/L,则H2的反应速率为0.03 mol/(L·min)
D.当反应吸收热量0.025Q kJ时,生成的HCl通入含0. 1 mol NaOH的溶液恰好反应
【答案】D
【解析】
试题分析:A.由于该反应的正反应是气体体积增大的反应,当反应达平衡后,若压缩容器的体积,容器内气体压强增大,根据平衡移动原理,增大压强,化学平衡向气体体积减小的逆反应方向移动,因此SiCl4的转化率减小,A错误;B.若反应开始时投入1mol SiCl4、2mol H2,由于该反应是可逆反应,反应物不能完全转化为生成物,因此达到平衡时吸收热量小于Q kJ,B错误;C.若反应4min HCl的浓度为0.12mol·L-1,则反应消耗的H2的浓度是0.06mol/L,由于反应时间没有给出,因此不能计算反应速率的大小,C错误;D.当反应吸收热量为0.025 Q kJ时,则生成的HCl的物质的量是(0.025 Q kJ÷QkJ)×4mol=0.1mol,根据反应方程式HCl+NaOH=NaCl+H2O可知0.1molHCl完全反应需要NaOH的物质的量是0.1mol,因此产生的气体全部通入100mL1mol·L-1的NaOH溶液中恰好反应,D正确。答案选D。


科目:高中化学 来源: 题型:
【题目】某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g。
(2)从图6中选择称量NaOH固体所需要的仪器是(填字母): 。

Ⅱ.测定中和热的实验装置如图7所示。
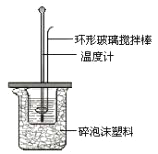
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式 (中和热数值为57.3 kJ/mol):
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃[ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H= (取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(3)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察右图,然后回答问题。
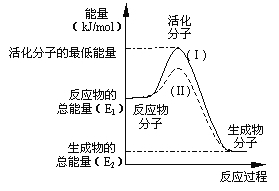
①图中所示反应是_________(填“吸热”或“放热”)反应,该反应的△H=____________(用含E1、E2的代数式表示)。
②对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式 。
②直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x= (用n表示)。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
□H2PO2-+□Ag+ + □ = □PO43-+ □Ag +□
(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下

①除砷过程在75℃下进行,其合理的原因是_______(填字母)。
a.温度不宜过高,防止硝酸分解 b.适当提高温度,加快化学反应速率
c.使白磷熔化,并溶于水 d.降低白磷的毒性
②硝酸氧化除砷时被还原为NO,若氧化产物为等物质的量的亚砷酸与砷酸,则化学反应方程式为_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A. ①② B. ①③ C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应中属于加成反应的是
A. 苯和液溴在FeBr3催化作用下反应生成溴苯
B. 乙烯使酸性高锰酸钾溶液褪色
C. 乙烯与HC1气体反应生成一氯乙烷
D. 丙烯和氯气在一定条件下反应生成CICH2CH =CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法正确的是
A.氯气可用于自来水消毒 B.甲醛可用作食品防腐剂
C.碳酸钠可用来治疗胃酸过多 D.铝制容器可长期存放碱性物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在①178O、1②188O、③2311Na、④2412Mg、⑤146C、⑥147N中:
(1)和互为同位素(填序号,下同);
(2)和的质量数相等,但不能互称同位素;
(3)和的中子数相等,但质子数不等,所以不是同一种元素.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在生产和生活中有广泛的应用。
Ⅰ.NO2与SO2都是形成酸雨的主要物质。在一定条件下,两者能发生反应:
NO2(g)+SO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
(1)在一定条件下,将等物质的量的NO2、SO2气体置于体积固定的密闭容器中发生反应,下列能说明反应已经达到平衡状态的是
a.v(NO2)生成=v(SO2)消耗
b.混合气体的总压强不再改变
c.容器内气体颜色不再改变
d.容器内气体平均相对分子质量不再改变
(2)科学家正在研究利用催化技术将NO2和CO转变成无害的CO2和N2,反应的化学方程式:
2NO2(g)+4CO(g)![]() 4CO2(g)+N2(g)+Q(Q>0)
4CO2(g)+N2(g)+Q(Q>0)
若在密闭容器中充入NO2和CO,下列措施能提高NO2转化率的是 。
A.选用高效催化剂 B.充入NO2 C.降低温度 D.加压
Ⅱ.(1)17℃、1.01×105Pa,在2L密闭容器NO2和N2O4的混合气体达到平衡时,NO2的物质的量为0.2mol,N2O4的体积分数为6/11。计算该条件下反应2NO2(g)![]() N2O4(g)的平衡常数K= 。若此时向容器中再充入0.1mol NO2和0.12mol N2O4,原化学平衡 移动(填“正向”、“逆向”或“不”)。
N2O4(g)的平衡常数K= 。若此时向容器中再充入0.1mol NO2和0.12mol N2O4,原化学平衡 移动(填“正向”、“逆向”或“不”)。
(2)现用一定量的Cu与足量的浓HNO3反应,制得2.20L(已折算到标准状况)已达到平衡的NO2 和N2O4的混合气体,理论上至少需消耗Cu g(保留两位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com