
为探究某铁碳合金与浓硫酸在加热条件下反应的部分产物并测定铁碳合金中铁元素的质量分数,某化学活动小组设计了下图所示的实验装置,并完成以下实验探究。

往圆底烧瓶中加入mg铁碳合金,并滴入过量浓硫酸,点燃酒精灯。
(1)装置B的作用是______________________________________。
(2)甲同学观察到装置C中有白色沉淀生成。他得出了使澄清石灰水变浑浊的气体是二氧化碳的结论。装置A中能产生二氧化碳的化学方程式为_______________。
(3)乙同学认为甲同学的结论是错误的,他认为为了确认二氧化碳的存在,需在装置B~C之间添加装置M,装置E、F中盛放的试剂分别是_____、__________。重新实验后观察到装置F中的现象是_______________________________。
(4 )有些同学认为合金中铁元素的质量分数可用KMnO4溶液来测定
(5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)
测定铁元素质量分数的实验步骤如下:
I.往烧瓶A中加入过量的还原剂铜粉使溶液中的Fe3+完全转化为Fe2+过滤,得到滤液B;
II.将滤液B稀释为250 mL;
III.取稀释液25.00 mL,用浓度为c mol·L-1的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为VmL。
①步骤II中,将滤液B稀释为250 mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是___________________。
②滴定过程中_______________(填“需要”或“不需要")加入指示剂。
③铁碳合金中铁元素的质最分数为_____________________________。
【知识点】铁碳合金与浓硫酸在加热条件下反应的实验探究J4
【答案解析】(1)检验SO2的存在
(2)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(3)酸性KMnO4溶液或溴水(或其他合理答案) 品红溶液 品红溶液不褪色或无明显现象
(4)①250 mL容量瓶(1分) ②不需要(1分) ③
解析:(1)根据装置B中的试剂是品红溶液,即可知道装置B的作用是检验SO2的存在。
(2)装置A中碳与浓硫酸反应能产生二氧化碳,化学方程式为C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(3)乙同学认为甲同学的结论是错误的,因为二氧化硫也能使石灰水变浑浊,为了确认二氧化碳的存在,需在装置B~C之间添加装置M,除去SO2并证明SO2已除净,所以装置E中盛放的试剂是酸性KMnO4溶液或溴水 ,F中盛放的试剂分别是品红溶液。重新实验后观察到装置F中的现象是品红溶液不褪色或无明显现象。
(4)①将滤液B稀释为250 mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是250 mL容量瓶, ②滴定终点时溶液由无色变紫色,溶液有颜色变化所以不需要加入指示剂。
③铁碳合金中铁元素的质最分数为:

【思路点拨】本题考查了铁碳合金与浓硫酸在加热条件下反应的实验探究,但多为课本内容,较简单。


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是

A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl2·4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是 ( )
A.13C和14C属于同 一种元素,它们互为同位素
一种元素,它们互为同位素
B.1H和2H是不同的核素,它们的质子数相等
C.14C和14N的质量数相等,它们的中子数不等
D.6Li和7Li的核外电子数相等,中子数也相等
查看答案和解析>>
科目:高中化学 来源: 题型:
利用反应2NO(g)+2CO(g)  2CO2(g)+N2(g) ΔH=-746.8 kJ/mol,可净化汽车尾气,如果要同时
2CO2(g)+N2(g) ΔH=-746.8 kJ/mol,可净化汽车尾气,如果要同时
提高该反应的速率和NO的转化率,采取的措施是( )
A.降低温度
B.增大压强同时加催化剂
C.升高温度同时充入N2
D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应3A(g)+B(g)  xC(g)+2D(g),
xC(g)+2D(g),
经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min).求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=________mol.
(2)B的平均反应速率v(B)=________mol/(L·min).
(3)x的值为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
[选做题]本题有A、B两题,分别对应于“物质结构与性质”和“实验化学”两个选修课程模块的内容,每题12分。请选择其中一题作答,若两题都作答。将按A题评分。
A.【物质结构与性质】
可以由下列反应合成三聚氰胺:CaO+3C CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2  CN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式: 。 CaCN2中阴离子为CN ,根据等电子原理可以推知CN
,根据等电子原理可以推知CN 的空间构型为 。
的空间构型为 。
 (2)尿素分子中C原子采取 杂化。尿素分子的结构简式是 。
(2)尿素分子中C原子采取 杂化。尿素分子的结构简式是 。
(3)三聚氰胺( )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸( )
后,三聚氰酸与三聚氰胺分子相互之间通过 结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为 。


(5)CaO晶体和NaCl晶体的晶格能分别为:CaO 3401 kJ·mol-1、NaCl 786 kJ·mol-1。导致CaO比NaCl晶格能大的主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在实验室中模拟石油的催化裂化,装置如图:实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实验后闻试管Ⅱ中液体气味,具有汽油的气味。
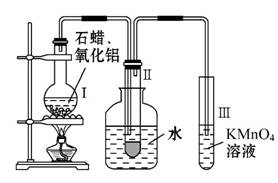
(1)该装置仪器连接的顺序应遵循的原则为 ,加入药品之前的操作为 ,长导管的作用是 。
(2)试管Ⅱ中少量液体凝结说明了 。
(3)试管Ⅲ中溶液褪色说明了 。
(4)能否用试管Ⅱ中的液体萃取溴水中的溴,理由是
。
(5)写出二十烷裂化得到癸烷和癸烯的化学方程式
。
(6)石油裂化的重要意义是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com