
【题目】a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物.b为EDTA与Ca2+形成的螯合物.下列叙述正确的是( ) 
A.b含有分子内氢键
B.b中Ca2+的配位数为4
C.b含有共价键、离子键和配位键
D.a和b中的N原子均为sp3杂化
【答案】D
【解析】解:A.b中N原子、O原子均未与H原子形成共价键,b中没有分子内氢键,故A错误; B.b为配离子,钙离子与N、O原子之间形成配位键,b中Ca2+的配位数为6,故B错误;
C.b为配离子,钙离子与N、O原子之间形成配位键,其它原子之间形成共价键,不含离子键,故C错误;
D.a中N原子形成3个σ键、含有1对孤对电子,而b中N原子形成4个σ键、没有孤对电子,N原子杂化轨道数目均为4,N原子均采取sp3杂化,故D正确;
故选D.
A.b中N原子、O原子均未与H原子形成共价键,没有氢键;
B.b中Ca2+的配位数为6;
C.b为配离子,钙离子与N、O原子之间形成配位键,其它原子之间形成共价键;
D.a中N原子形成3个σ键、含有1对孤对电子,而b中N原子形成4个σ键、没有孤对电子,N原子杂化轨道数目均为4.


科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是( )
A.气态氢化物的稳定性:H2O>NH3>SiH4
B.氢元素与其他元素可形成共价化合物或离子化合物
C.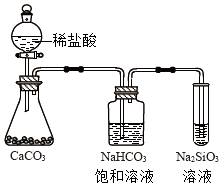
如图所示实验可证明元素的非金属性:Cl>C>Si
D.用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴有两种同位素,在自然界中各占一半,已知溴原子的质子数为35.溴的近似相对原子质量为80,则溴的两种同位素的中子数是.
A.19和81
B.45和46
C.44和45
D.44和46
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.根据所学知识,回答下列问题:
(1)元素周期表1~20号元素中,金属性最强的元素是______(填元素符号,下同);属于稀有气体的是_________;非金属性最强的元素在周期表中的位置是__________________。
(2)己知NO2和N2O4之间发生可逆反应:2NO2(g)(红棕色)![]() N2O4(g)(无色)。将装有NO2和N2O4混合气体的烧瓶浸入热水中,观察到的现象是_______,产生该现象的原因是________。
N2O4(g)(无色)。将装有NO2和N2O4混合气体的烧瓶浸入热水中,观察到的现象是_______,产生该现象的原因是________。
(3)一定条件下,向2L恒容密闭容器中按体积比1:3充入4.48L(标准状况)N2和H2的混合气体,发生反应N2(g)+3H2(g)![]() 2NH3(g),5min时反应达到平衡状态,测得c(N2)=0.02mol/L。
2NH3(g),5min时反应达到平衡状态,测得c(N2)=0.02mol/L。
①0~5min内,v(NH3)=_______________。
②下列叙述可证明上述反应达到平衡状态的是________(填序号)。
a.V(H2)=3v(N2)
b.容器内压强保持不变
c.每消耗ImolN2,同时生成2molNH3
d.N2、H2和NH3的物质的量浓度不再变化
II.五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C的简单离子和B的简单离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物中阴阳离子的个数比为1:1。回答下列问题:
(1)五种元素中,原子半径最大的是______(填元素名称),非金属性最强元素的是_________。
(2)由元素A分别和元素B、D、E所形成的共价型化合物中,热稳定性最差的是_____(用化学式表示)。
(3)元素A和E形成的化合物与元素A和B形成的化合物反应,产物的电子式为______,其中存在的化学键类型为______________。
(4)E离子的结构示意图是____________;元素D最高价氧化物的水化物的化学式为_____。
(5)单质E与水反应的离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍.回答下列问题:
(1)B2A4分子中B原子轨道的杂化类型为 , B2A4分子中σ键和π键个数比为 .
(2)A、B、C、D四种元素的电负性从大到小的顺序为(用元素符号表示);化合物CA3的沸点比化合物BA4的高,其主要原因是 .
(3)元素B的一种氧化物与元素C的一种氧化物互为等电子体,元素C的这种氧化物的分子式是 .
(4)元素E能形成多种配合物,如:E(CO)5等. ①基态E原子的价电子排布图为 .
②E(CO)5常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断E(CO)5晶体属于(填晶体类型),该晶体中E的化合价为 .
(5)E和C形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为 . 若两个最近的E原子间的距离为acm,则该晶体的密度是gmL﹣1 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室需要配制500mL 0.10mol/L Na2CO3溶液.
(1)所需玻璃仪器有:玻璃棒、烧杯、100mL量筒、
(2)实验时图中所示操作的先后顺序为(填编号)
(3)在配制过程中,下列操作对所配溶液浓度有无影响?(填“偏高”、“偏低”或“无影响”)
①称量时误用“左码右物”
②转移溶液后没有洗涤烧杯和玻璃棒
③向容量瓶加水定容时俯视液面
④摇匀后液面下降,再加水至刻度线
(4)所需Na2CO3固体的质量为g;若改用浓溶液稀释,需要量取2mol/L Na2CO3溶液mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制物质的量浓度均为0.2mol/L 的NaCl溶液和稀H2SO4 各480mL.提供的试剂是:NaCl固体和98%的浓H2SO4(密度为1.84g/cm3)及蒸馏水.
(1)应用托盘天平称量NaClg,应用10mL量筒量取H2SO4mL;
(2)配制两种溶液时都需要的仪器是;
(3)稀释浓H2SO4时应注意;
(4)在配制上述溶液实验中,下列操作引起结果偏低的有(填序号)
A.在烧杯中溶解溶质搅拌时,溅出少量溶液
B.没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
C.定容时,加水超过了刻度线,倒出一些再重新加水到刻度线
D.将所配溶液从容量瓶转移到试剂瓶时,有少量溅出
E.把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
F.容量瓶刚用蒸馏水洗净,没有烘干
G.量筒量取浓H2SO4后没有用蒸馏水洗涤2~3次,并将洗液移入容量瓶中.
H.容量瓶加水定容时俯视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,1.7g氨气所占的体积为 L,它与标准状况下 L硫化氢含有相同数目的氢原子.
(2)某气态氧化物的化学式为RO2 , 在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为 ,R的相对原子质量为 .
(3)已知CO、CO2的混合气体质量共16.0g,标准状况下体积为8.96L,则可推知该混合气体中含CO g,所含CO2在标准状况下的体积为 L.
(4)同温同压下,SO2与氦气的密度之比为 ;若质量相同,两种气体的体积比为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com