
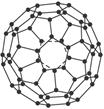
| A.C18 | B.C44 | C.C72 | D.C83 |
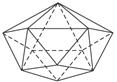
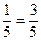 ,该基本结构单元中含硼原子数目为20×
,该基本结构单元中含硼原子数目为20× =12;又因为每条边(B—B键)为2个三角形所共有,因此,该基本结构单元中所含B—B键数目为20×3×
=12;又因为每条边(B—B键)为2个三角形所共有,因此,该基本结构单元中所含B—B键数目为20×3×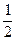 =30。若削去晶体硼结构单元中的一个顶角,则得到一个正五边形(数学上,一个平行于正五棱锥底面的平面与正五棱锥相截,所得截面为一正五边形)。因晶体硼结构单元中每一个顶角都为B原子所占有,晶体硼结构单元中共有12个硼原子,故一共可得12个正五边形。另外,一个等边三角形切去三个顶点后,得到正六边形,因晶体硼结构单元中共有20个等边三角形,故最终将得到20个正六边形。
=30。若削去晶体硼结构单元中的一个顶角,则得到一个正五边形(数学上,一个平行于正五棱锥底面的平面与正五棱锥相截,所得截面为一正五边形)。因晶体硼结构单元中每一个顶角都为B原子所占有,晶体硼结构单元中共有12个硼原子,故一共可得12个正五边形。另外,一个等边三角形切去三个顶点后,得到正六边形,因晶体硼结构单元中共有20个等边三角形,故最终将得到20个正六边形。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.构成离子晶体的作用力可能是离子键也可能是共价键 |
| B.氯化铯晶体是由氯化铯分子构成的 |
| C.由于离子的带电量有限,一个离子可以同时吸引的带相反电荷的离子数也有限 |
| D.一种离子化合物如果适合作耐高温材料,它的晶格能一定相当大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属原子半径都较大,价电子较少 |
| B.金属受外力作用后,金属离子与自由电子仍保持其较强的作用 |
| C.金属中的大量自由电子,受外力作用后,运动速度加快 |
| D.自由电子能迅速传递能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
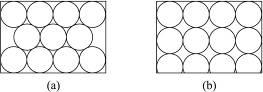
| A.图(a)为非密置层,配位数为6 |
| B.图(b)为密置层,配位数为4 |
| C.图(a)在三维空间里堆积可得镁型和铜型 |
| D.图(b)在三维空间里堆积仅得简单立方 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.LaNi6 | B.LaNi3 |
| C.LaNi4 | D.LaNi5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
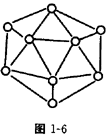
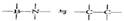 属等电子体物质,其结构和性质具有极大的相似性,则可推知,在BN的两种晶型中,一种是类似_________的空间网状结构晶体,可用作耐磨材料;另一种是类似于_________的层状结构的混合型晶体,可作用润滑材料,在其结构的每一层上最小的封闭环中有 _________个B原子,B—N键键角为_________。
属等电子体物质,其结构和性质具有极大的相似性,则可推知,在BN的两种晶型中,一种是类似_________的空间网状结构晶体,可用作耐磨材料;另一种是类似于_________的层状结构的混合型晶体,可作用润滑材料,在其结构的每一层上最小的封闭环中有 _________个B原子,B—N键键角为_________。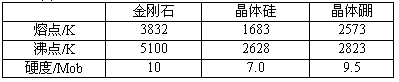
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔化状态下能导电的物质一定是离子化合物 |
| B.P4和NO2都是共价化合物 |
| C.在氧化钙和二氧化硅晶体中都不存在单个的小分子 |
| D.离子化合物中一定不存在单个的分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com