
| A、通入氧气的电极为正极 |
| B、参加反应的O2与C2H6的物质的量之比为7:2 |
| C、放电一段时间后,KOH的物质的量浓度将下降 |
| D、放电一段时间后,正极区附近溶液的pH减小 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、髙效等优良的性能.
甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、髙效等优良的性能.物质 | CH3OCH3(g) | H20(g) | |
| 浓度(mol?L-1) | 0.60 | 0.60 |
| 容器 | 甲2 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCO、4molH2 |
| CH3OH | c1=0.25 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | a1 | a2 | a3 |
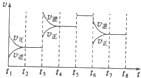
| t1-t2 | t4-t5 | t5-t6 | t7-t8 |
| K4 | K5 | K6 | K7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| B、氯化亚铁溶液与过氧化钠2:1反应:6Fe2++3Na2O2+6H2O═4Fe(OH)3↓+6Na++2Fe3+ |
| C、向氧化铁中加入氢碘酸发生反应:Fe2O3+6HI═2Fe2++I2+3H2O+4I- |
| D、过量铁粉与稀HNO3反应:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.10 | B、0.20 |
| C、0.30 | D、0.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO32-+H2O?HCO3-+OH-用热的纯碱溶液清洗油污 |
| B、Al3++3H2O?Al(OH)3+3H+明矾净水 |
| C、TiCl4+(x+2)H2O(过量)═TiO2?xH2O↓+4HCl 制备TiO2纳米粉 |
| D、SnCl2+H2O═Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用盐酸或NH4Cl溶液可溶解Mg(OH)2沉淀 |
| B、可用氨水鉴别AlCl3、AgNO3和CuSO4三种溶液 |
| C、附着在试管内壁上的AgCl固体可用氨水溶解而洗去 |
| D、除干燥CO2中混有的少量SO2可将混合气体通过盛有酸性KMnO4的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com