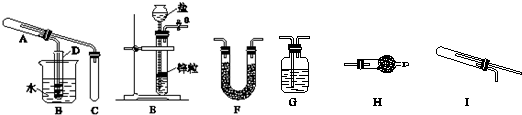
ʵ�飺��һ����װ�üס��ҡ������齺�����һ��װ�ã��������Ѽ�飩����������ȡ���ռ�NH
3��HCl���壮�ɹ�ѡ���Һ���Լ��У�Ũ���ᡢϡ���ᡢŨ���ᡢϡ���ᡢŨ��ˮ�������Լ�Ϊ��ɫʯ����Һ����ش��������⣮
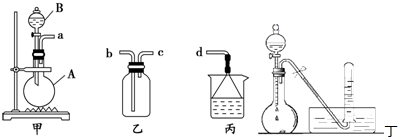
������ȡij����Ĺ����У����е�ʯ����Һ��죬����ƿA�е��Լ����Һ©��B�е��Լ���Ϊ��ɫҺ�壬����ƿA�е��Լ�Ϊ
����ȡ�����������˷�Һ©��B���Լ���������
��
��ͨ��������ɫʯ����Һ���������˵�����������Ѽ�������ʯ����Һ����������ƿA��Ӧ����Ĺ����Լ�Ϊ
��
�����������ռ���������������װ�õ�˳���ǣ�a��
��
��d����ӿڴ��ţ���
��������Ԫ�ؼ��仯�����������������й㷺Ӧ�ã�
��1��ijУ��ѧʵ��С��ͬѧ�����й�NO
2�����ϵ��ʵ�飨��ͼ���� ʾ������ƿ�з�������ͭƬ����Һ©�����������������Ũ���ᣬ�Թ����ռ���������ɫ��
���û�ѧ����ʽ��ʾ�����ɫ��ԭ����
������ƿ�����ˮ�У���ƿ��������ɫ
�������������䡱��dz��������ɫ�仯��ԭ����
���û�ѧ����ͱ�Ҫ����˵������
��2����֪��N
2��g��+3H
2��g��?2NH
3��g����H=-92kJ?mol
-1�������йظ÷�Ӧ���ʵ���������ȷ���ǣ�ѡ����ţ�
��
a�������¶ȿ����������Ӱٷ������ӿ췴Ӧ����
b������ѹǿ�����������Ӱٷ����������Լӿ췴Ӧ����
c��ʹ�ô�������ʹ��Ӧ�����ƽ���������ߣ��ӿ췴Ӧ����
d��������һ��������£����������ı������С���Է�Ӧ����������Ӱ��
�ڸ����¶ȶԻ�ѧƽ���Ӱ����ɿ�֪�����ڸ÷�Ӧ���¶�Խ�ߣ���ƽ�ⳣ����ֵԽ
��
��ij�¶��£�����10mol N
2��30mol H
2 �������Ϊ10L���ܱ������ڣ���Ӧ�ﵽƽ��״̬ʱ�����ƽ���������а����������Ϊ20%������¶��·�Ӧ��K=
�����÷�����ʾ����
��3����ͳ�ĺϳɰ���ҵ��Ҫ���¸�ѹ�����ķ�Ӧ���������������ϱ����ڳ�ѹ�¿��õ�ⷨ�ϳɰ���ת���ʸߴ�78%����֪�·��ϳɰ������õĵ�����ܴ���H
+������������Ӧʽ��
��������Ӧʽ��
��




 �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д� ��������ϵ�д�
��������ϵ�д�