
| A. | 11H | B. | 12H | C. | -10e | D. | 01n |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 1mol乙基(-CH2CH3)中含有共价键的总数为7NA | |
| B. | 1L 0.1mol/L盐酸溶液所含HCl的分子数为NA | |
| C. | 标准状况下,11.2L NO2气体中含有的分子数为0.5NA | |
| D. | 标况下11.2L CO和CO2混合气体中,所含碳原子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
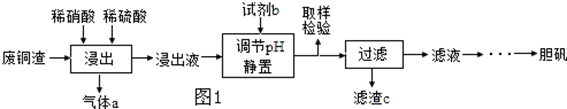
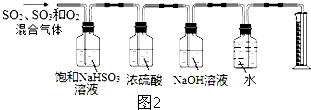
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
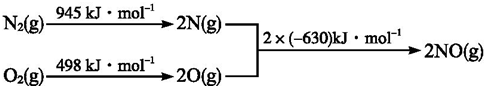
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应鉴别NaCl溶液和KCl溶液 | |
| B. | 向某溶液中加入BaCl2溶液出现白色沉淀,则该溶液中肯定有SO42- | |
| C. | 用KSCN溶液鉴别FeCl2溶液和Fe2(SO4)3溶液 | |
| D. | 用焰色反应可鉴别出NaCl、KCl和Na2SO4三种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 +HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$
+HNO3(浓)$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  打磨磁石制指南针 | B. |  烧结粘土制陶瓷 | ||
| C. |  湿法炼铜 | D. |  铁的冶炼 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


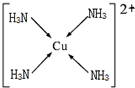 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com