
在室温下pH=12的某溶液中,由水电离的c(OH-)为( )
A.1.0×10-7 mol•L-1
B.1.0×10-6 mol•L-1
C.1.0×10-2 mol•L-1
D.1.0×10-12 mol•L-1
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:021
A.1.0×10-7 mol•L-1
B.1.0×10-6 mol•L-1
C.1.0×10-2 mol•L-1
D.1.0×10-12 mol•L-1
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山西省大同市实验中学高二上学期期中考试化学试卷 题型:填空题
(1)室温下PH=2的某强酸稀释100倍,PH=_____,PH=12的某强碱稀释100倍,PH=____
(2)室温下,PH=2的HCl与PH=12的氨水等积混合后,溶液的PH_ __7(填>,<或=),原因是 _______________________________________________________________________________
__7(填>,<或=),原因是 _______________________________________________________________________________
(3)室温下,0.01mol/L的HCl与0.01mol/L的氨水混合后,溶液的PH___7(填>,<或=),原因是_______________________________________________________________________
(4)室温下,将PH=5的H2SO4溶液稀释10倍C(H+):C(SO42-)=_________
将稀释后的溶液再稀释100倍,C(H+):C(SO42-)=_________
(5)MOH和ROH两种一元碱的水溶液分别加水稀释时,PH变化如右图:下列叙述中正确的是()
A:MOH是一种弱碱
B:在x点,MOH完全电离
C:在x点C(M+)=C(R+)
D:稀释前ROH溶液中C(OH-)是MOH溶液中C(OH-)的10倍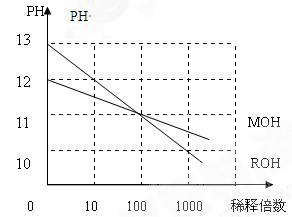
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在室温下pH=12的NaOH溶液100ml,要使它的pH变为11。
①如果加入蒸馏水,应加_____________ml
②如果加入pH=10的NaOH溶液, 应加____________ml
③如果加入0.01mol/L盐酸, 应加_________ml
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡________移动(填“向左”“向右”或“不”);若加入少量下列试剂中的_______(填序号),产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHCO3 e. CH3COONa
(3)25℃时,向纯水中加入Na2CO3,测得溶液的pH=10,则由水电离出的OH-离子浓度与溶液中的H+离子浓度之比为_____________
(4)已知:下列两个热化学方程式:
Fe(s) + 1/2O2(g) ![]() FeO(s) △ H=-272.0KJ/mol
FeO(s) △ H=-272.0KJ/mol
2Al(s) + 3/2O2(g) ![]() Al2O3(s) △H=-1675.7KJ/mol
Al2O3(s) △H=-1675.7KJ/mol
则 Al(s)的单质和FeO(s)反应的热化学方程式是___________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com