
| A. | 1.0 mol•L-1的KNO3溶液中:Fe2+、H+、Cl-、I- | |
| B. | 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN- | |
| C. | 常温下,在c(H+)/c(OH-)=1×1012的溶液:NH4+、Mg2+、C1-、K+ | |
| D. | 水电离的c(H+)=1×10-13 mol•L-1的溶液中:K+、Na+、AlO2-、CO32- |
分析 A.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子、碘离子;
B.铁离子与硫氰根离子反应;
C.常温下,在c(H+)/c(OH-)=1×1012的溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应;
D.水电离的c(H+)=1×10-13 mol•L-1的溶液中存在大量氢离子或氢氧根离子,偏铝酸根离子、碳酸根离子与氢离子反应.
解答 解:A.KNO3在酸性条件下具有强氧化性,能够氧化Fe2+、I-,在溶液中不能大量共存,故A错误;
B. Fe3+和 SCN-反应生成硫氰化铁,在溶液中不能大量共存,故B错误;
C.常温下,在c(H+)/c(OH-)=1×1012的溶液呈酸性,溶液中存在大量氢离子,NH4+、Mg2+、C1-、K+之间不反应,都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.水电离的c(H+)=1×10-13 mol•L-1的溶液呈酸性或碱性,AlO2-、CO32-与氢离子反应,在酸性溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等.


科目:高中化学 来源: 题型:解答题
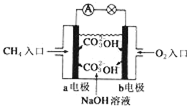 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ②③④⑤ | C. | ②④⑤⑥⑦ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业制氧、钢铁生锈 | B. | 石蜡熔化、干冰升华 | ||
| C. | 粮食酿酒、烟花燃放 | D. | 汽油挥发、云消雾散 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯 | B. | 丙炔 | C. | 丁二烯 | D. | 甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | CaCl2 | C. | AlCl3 | D. | MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
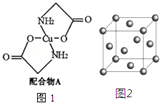 已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A.其结构如图1所示
已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A.其结构如图1所示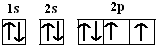 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com