
| A、通常情况下,22.4L乙烯中C-H键数为4NA |
| B、1mol羟基中电子数为10NA |
| C、在反应KIO3+6HI═KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
| D、常温下,1L 0.1mol?L-1的NH4NO3溶液中氮原子数为0.2NA |


科目:高中化学 来源: 题型:
| A、Na+、Cl-、K+、SiO32- |
| B、Na+、CO32-、Fe2+、NO3- |
| C、K+、SO42-、Cl-、Cu2+ |
| D、Na+、NO3-、Al3+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、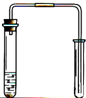 用铜和稀硝酸制取少量NO |
B、 制取并收集氨气 |
C、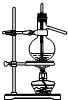 蒸馏法分离水和酒精 |
D、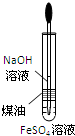 制备Fe(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
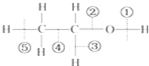 乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说明是:
乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说明是:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
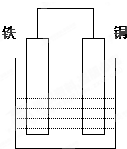 在以铁、铜为两电极的原电池中,如图所示:
在以铁、铜为两电极的原电池中,如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com