

分析 (1)仪器A是分液漏斗,B为圆底烧瓶;
(2)有连接的实验装置在加入药品前要进行气密性检验;烧瓶中Cu与浓硫酸反应生成硫酸铜、二氧化硫和水;
(3)①二氧化硫和碳酸氢钠反应生成亚硫酸钠、二氧化碳和水;
②元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
③碳酸制备硅酸,说明碳酸的酸性大于硅酸,即说明碳元素的非金属性强于硅元素.
解答 解:(1)仪器A是分液漏斗,分液漏斗能控制液体流速,B是圆底烧瓶;
故答案为:分液漏斗;圆底烧瓶;
(2)有连接的实验装置在加入药品前要进行气密性检验,否则实验不成功;烧瓶中Cu与浓硫酸反应生成硫酸铜、二氧化硫和水,其反应方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
故答案为:检验装置气密性;Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(3)①二氧化硫和碳酸氢钠反应生成亚硫酸钠、二氧化碳和水,其反应的离子方程式为:2HCO3-+SO2=2CO2+SO32-+H2O;
故答案为:2HCO3-+SO2=2CO2+SO32-+H2O;
②元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,所以气体通过D装置发生2HCO3-+SO2=2CO2+SO32-+H2O,说明亚硫酸的酸性大于碳酸,但是亚硫酸不是最高价氧化物的水化物,所以不能根据亚硫酸与碳酸的酸性来判断非金属性;
故答案为:亚硫酸不是硫的最高价氧化物对应水化物,故酸性强于碳酸不能说明硫的非金属性强;
③酸性强的酸能和弱酸盐反应生成弱酸,二氧化碳和硅酸钠反应生成难溶性的硅酸,导致G中溶液变浑浊,所以说明碳酸酸性大于硅酸,即碳元素的非金属性强于硅元素;
故答案为:有白色沉淀生成.
点评 本题考查了探究实验方案设计,明确非金属性强弱与其最高价含氧酸酸性强弱关系、强酸制取弱酸原理即可解答,知道图中各仪器的作用,侧重考查学生分析问题、解答问题能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 常温下都不可用铝制容器贮存 | |
| B. | 常温下都能与铜较快反应 | |
| C. | 露置于空气中,溶液浓度均降低 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式为CH2CH2 | B. | CO2分子的结构式:O=C=O | ||
| C. | 过氧化氢的电子式: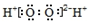 | D. | 四氯化碳分子比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2分子的电子式为: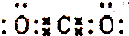 | |
| B. | 质子数为x,中子数为y的氧元素的核素符号为${\;}_{x}^{x+y}$O | |
| C. | Cl-的离子结构示意图为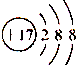 | |
| D. | HClO的结构式为H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为p轨道是“8”字形的,所以p电子走“8”字形 | |
| B. | 第三电子层,有3s、3p、3d三个轨道 | |
| C. | 在一个基态多电子的原子中,不可能有两个能量完全相同的电子 | |
| D. | 一般情况下,σ键比π键重叠程度大,形成的共价键强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①④ | B. | 只有③⑤ | C. | 只有②③ | D. | 只有①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同素异形体 | |
| B. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同位素 | |
| C. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se物理性质和化学性质均相同 | |
| D. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se都含有34个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在熔融电解质中,O2-由负极移向正极 | |
| B. | 通入空气的一极是正极,电极反应为:O2+2H2O+4e-═4OH- | |
| C. | 通入甲烷的一极是负极,电极反应为:CH4+8e-+4O2-═CO2+2H2O | |
| D. | 当电路中通过amol电子时,理论上能生成标准状况下CO2气体2.8aL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com