
四种短周期元素的性质或结构信息如下表。下列推断错误的是
|
元素编号 |
元素性质或结构 |
|
T |
M层上有2对成对电子 |
|
X |
元素最高正价是+7价 |
|
Y |
第三周期元素的简单离子中半径最小 |
|
Z |
单质是银白色固体、导电、密度比水小,与水剧烈反应、和氧气反应不同条件下产物不同 |
A.T的氢化物是同族元素氢化物中沸点最低的
B.X的最高价氧化物对应的水化物,是无机含氧酸中的最强酸
C.离子半径从小到大的顺序:Y<Z< T < X
D.X、Y形成化合物的晶体类型与X、Z形成化合物的晶体类型不同
C
【解析】
试题分析:M层上有2对成对电子,说明T是S元素;元素最高正价是+7价,因此X是氯元素;第三周期元素的简单离子中半径最小的是铝,则Y是Al;根据Z的性质以及和氧气的产物可判断,Z是Na。A不正确,因为水分子间存在氢键,所以沸点是同族元素氢化物中沸点最高,而H2S的最低,A正确;高氯酸是已知含氧酸中酸性最强的,B最强;核外电子排布相同的离子,其离子半径随原子序数的递增而减小,C不正确,离子半径从小到大的顺序是Y<Z<X<T;氯化铝形成的晶体是分子晶体,氯化钠形成的晶体是离子晶体,D正确,答案选C。
考点:考查元素周期律的判断和应用
点评:该题是高考中的常见题型,属于中等难度的试题,试题难易适中,侧重学生能力的考查。该题有利于培养学生严谨的逻辑思维能力,有利于提高学生的学习效率和应试能力。


科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质或结构信息 | 室温下单质呈粉末状固体,加热易熔化;单质在氧气中燃烧发出明亮的蓝紫色火焰 | 单质在常温、常压下是气体,能溶于水;原子的M层比L层少1个电子 | 单质为质软、银白色固体,导电性强;单质在空气中燃烧发出黄色火焰 | 原子的最外电子层上电子数比内层电子总数少6;单质为空间网状晶体,具有很高的熔沸点 |


查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质 结构 信息 |
室温下单质呈粉末状固体,加热易熔化. 单质在氧气中燃烧,发出明亮的蓝紫色火焰. |
单质常温、常压下是气体,能溶于水. 原子的M层有1个未成对的p电子. |
单质质软、银白色固体、导电性强. 单质在空气中燃烧发出黄色的火焰. |
原子最外层电子层上s电子数等于p电子数. 单质为空间网状晶体,具有很高的熔、沸点. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质或 结构 信息 |
室温下单质为黄色粉末状固体,加热易熔化;单质在氧气中燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体 | 单质常温、常压下是气体,能溶于水;原子的M层上有7个电子 | 单质质软、银白色固体、导电性强;单质在空气中燃烧发出黄色的火焰,生成淡黄色的固体 | 原子最外电子层有4个电子;其单质既能与酸反应,又能与碱反应 |
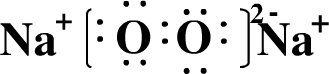
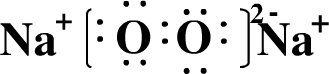
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质 结构 信息 |
室温下单质是粉末状固体,加热易熔化. 单质在空气中燃烧生成的气体是形成酸雨的主要污染物之一. |
单质常温、常压下是黄绿色气体,能溶于水. | 单质质软、银白色固体、导电性强. 单质在空气中燃烧发出黄色的火焰. |
原子最外层电子层上s电子数等于p电子数. 单质是一种常见的半导体材料. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层上的电子数是原子核外电子层数的2倍 |
| X | 最外电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 最高正化合价是+7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com