
【题目】计算多元弱酸(HnX)溶液的c(H+)及比较弱酸的相对强弱时,通常只考虑第一步电离。回答下列关于多元弱酸HnX的问题。
(1)若要使HnX溶液中c(H+)/c(HnX)增大,可以采取的措施是__________。
A.升高温度 B.加少量固态HnX C.加少量NaOH溶液 D.加水
(2)用离子方程式解释NanX呈碱性的原因:______________________________。
(3)若HnX为H2C2O4,且某温度下,H2C2O4的K1=5×10-2、K2=5×10-5.则该温度下,0.2mol/L H2C2O4溶液中c(H+)约为__________mol/L。(精确计算,且己知![]() )
)
(4)已知KHC2O4溶液呈酸性。
①KHC2O4溶液中,各离子浓度由大到小的顺序是____________________。
②在KHC2O4溶液中,各粒子浓度关系正确的是__________。
A.c(C2O42-)<c(H2C2O4)
B.c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)
C.c(K+)+c(H+)=c(OH-)+c(HC2O42-)+2c(C2O42-)
D.c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4)
【答案】(1)AD
(2)Xn-+H2O![]() X(n-1)-+OH-
X(n-1)-+OH-
(3)0.078
(4)①c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-) ②CD
【解析】
试题分析:(1)弱电解质的电离为吸热过程,升温促进电离,则c(H+)/c(HnX)比值增大,A项正确;加少量固态HnX,HnX浓度增大,弱电解质的浓度越大,电离程度越小,则c(H+)/c(HnX)比值减小,B项错误;加入NaOH溶液,消耗氢离子,使c(H+)减小,则c(H+)/c(HnX)比值减小,C项错误;加水,溶液体积增大,导致氢离子、醋酸浓度都减小,但是电离平衡向正向移动,氢离子浓度减的少,HnX浓度减得大,c(H+)/c(HnX)比值增大,D项正确;答案选AD。
(2)HnX是弱酸,Xn-在水溶液中存在水解平衡:Xn-+H2O![]() X(n-1)-+OH-,所以NanX溶液呈碱性。
X(n-1)-+OH-,所以NanX溶液呈碱性。
(3)K1=c(H+)c(HC2O4-)÷c(H2C2O4) =5×10-2、K2=c(H+)c(C2O42-)÷c(HC2O4-)=5×10-5,解得,c(H+)=0.078mol/L;
(4)①KHC2O4溶液呈酸性,说明草酸氢根离子的电离程度大于其水解程度,所以溶液显酸性,c(H+)>c(OH-) 溶液中离子浓度大小为c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);
② HC2O4-电离程度大于水解程度,c(C2O42-)>c(H2C2O4),A项错误;在KHC2O4溶液中,电荷守恒关系式为c(K+)+c(H+)=c(OH-)+c(HC2O42-)+2c(C2O42-),物料守恒关系式为c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4),C、D正确;由电荷守恒关系式和物料守恒关系式得c(C2O42-)+c(OH-)=c(H+)+c(HC2O4-)+ 2c(H2C2O4),B项错误;答案选CD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列描述中不正确的是( )
A. CS2为Ⅴ形的极性分子 B. ClO3-的空间构型为三角锥形
C. SF6中有6对完全相同的成键电子对 D. SiF4和SO32-的中心原子均为sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示,如CH3-CH=CH-CH3可简写为![]() 。有机物X的键线式为
。有机物X的键线式为![]() ,Y是X的同分异构体,且属于芳香烃。下列有关Y的说法正确的是( )
,Y是X的同分异构体,且属于芳香烃。下列有关Y的说法正确的是( )
A.Y能使酸性KMnO4溶液褪色,所以是苯的同系物
B.Y能使溴水褪色,且静置后不分层
C.Y不能发生取代反应
D.Y能发生加聚反应生成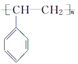
查看答案和解析>>
科目:高中化学 来源: 题型:
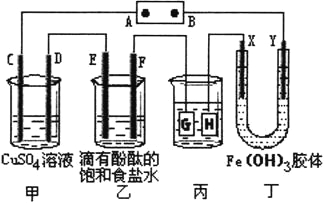
【题目】如下图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深。请回答:
(1)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为__________。
(2)现用丙装置给铜件镀银,当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为__________。
(3)Fe(OH)3胶体的制备有严格的要求,小明想向FeCl3溶液中滴加NaOH溶液来制备Fe(OH)3胶体,结果很快就生成了红褐色的沉淀。他测得溶液的pH=5,则此时溶液中c(Fe3+)=__________mol/L。(己知Ksp[Fe(OH)3]=1×10-36)。
(4)若用甲烷燃料电池(电解质溶液为2L2mol/LKOH溶液)提供电源,持续通入甲烷,在标准状况下,消耗甲烷的体积VL。当消耗CH4的体积在44.8<V≤89.6时,此时电源中B极发生的电极反应为:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水三氯化铁易升华,有强烈的吸水性,是一种用途比较广泛的盐。
(1)实验室中可将FeCl3溶液 、 、过滤、洗涤干燥得FeCl3·6H2O;再 ,得到无水FeCl3。
(2)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)= mol·L-1(已知:Ksp[Fe(OH)3]= 1.1×10-36)。
(3)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:
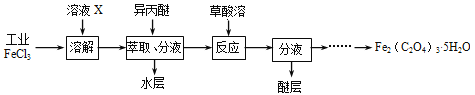
①为抑制FeCl3水解,溶液X为 。
②上述流程中FeCl3能被异丙醚萃取,其原因是 ;检验萃取、分液后所得水层中是否含有Fe3+的方法是 。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是 。
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于右图所示仪器 (填“甲”或“乙”)中;下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是 。
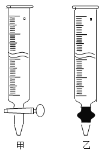
a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据碘与氢气反应的热化学方程式(碘为气态或固态),下列判断正确的是( )
(ⅰ) I2(?)+H2(g) ![]() 2HI(g) △H=-9.48 kJ/mol
2HI(g) △H=-9.48 kJ/mol
(ⅱ) I2(?)+H2(g) ![]() 2HI(g) △H=26.48 kJ/mol
2HI(g) △H=26.48 kJ/mol
A.ⅰ中碘为气态,ⅱ中碘为固态
B.反应(ⅰ)的产物比反应(ⅱ)的产物稳定
C.1 mol I2(g)中通入1 mol H2(g),反应放热9.48 kJ
D.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 。
(2)液氨是富氢物质,是氢能的理想载体,利用![]() 2NH3实现储氢和输氢。下列说法正确的是 。
2NH3实现储氢和输氢。下列说法正确的是 。
a.NH3分子中氮原子的轨道杂化方式为sp2杂化 b.电负性顺序:C<N<O<F
c.由于氨分子间存在氢键,所以稳定性:NH3>PH3 d.[Cu(NH3)4]2+中N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是 。
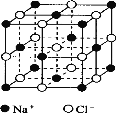
Ⅱ.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示:
(1)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则该Na+与跟它次近邻的Cl-的个数为 ,该Na+与跟它次近邻的Cl-之间的距离为 。
(2)已知在氯化钠晶体中Na+的半径为a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为 (用含a、b的式子表示)。
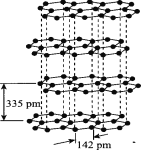
(3)硅与碳是同主族元素,其中石墨为混合型晶体,已知石墨的层间距为335 pm,C--C键长为142 pm,则石墨晶体密度约为 (列式并计算,结果保留三位有效数字,NA为6.02×1023 mol-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组以苯甲酸为原料制取苯甲酸甲酯。有关物质的沸点和相对分子质量如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
相对分子质量 | 32 | 122 | 136 |
Ⅰ.合成苯甲酸甲酯粗产品
在烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约0.79g/mL),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品
(1)混合液体时最后加入浓硫酸的理由是_____________________,浓硫酸的作用是_____________,若反应产物水分子中间有同位素18O,写出能表示反应前后18O位置的化学方程式____________;
(2)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是____________;
(3)甲、乙、丙三位同学分别设计了如图1三套实验室制取苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的特点,最好采用装置________(填“甲”、“乙”、“丙”)。 
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用图2流程图进行精制,请根 据流程图填入恰当操作方法的名称:操作I为_______,操作Ⅱ为 _______;
(5)通过计算,苯甲酸甲酯的产率为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(l)由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置乙中正极的电极反应式是 。
②四种金属活动性由强到弱的顺序是 。
(2)由Zn一Cu一硫酸溶液组成的原电池,工作一段时间后锌片的质量减少了6.5g.回答下列问题:溶液中的H+移向 (填“正极”或“负极’) 。负极的电极反应式是 , 标准状况下生成 L气体。
(3)断开1 mol H一H键、1 mol N一H键、1 mol N≡N 键分别需要吸收能量为436KJ、391KJ、946KJ,求:H2与N2反应生成0.5 molNH3填(“吸收”或“放出”)能量 KJ。
(4)原子序数大于4的主族元素A和B的离子分别为Am+和Bn-,已知它们的核外电子排布相同,据此推断:
① A和B所属周期数之差为(填具体数字) 。
② A和B的核电荷数之差为(用含m或n的式子表示) 。
③ B和A的族序数之差为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com